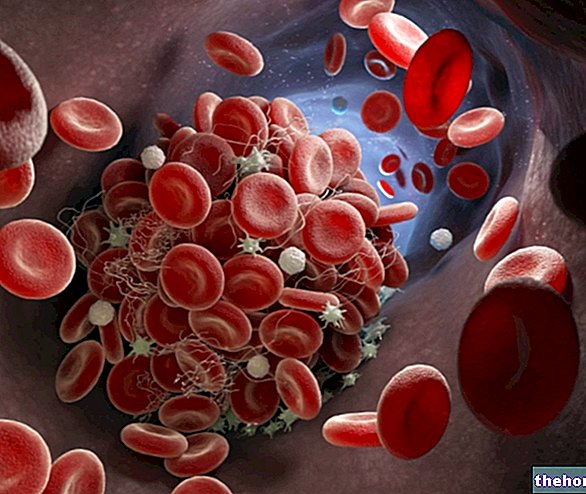
2،3 ثنائي فسفوغليسيرات (2،3 DPG) هو مركب مشتق من منتج وسيط لتحلل السكر ؛ يتركز بشكل خاص على مستوى كريات الدم الحمراء ، لأن خلايا الدم الحمراء - التي تخلو من الميتوكوندريا - تستغل استقلاب اللاكتات اللاهوائي (التخمير المثلي للجلوكوز) للحصول على الطاقة.

الهيموجلوبين عبارة عن بروتين رباعي ، يتكون من أربع وحدات فرعية ، وحدتان من ألفا واثنان بيتا ، يتكون كل منها من جزء بروتين (غلوبين) وهيم (مجموعة صناعية تربط الأكسجين). يرتبط 2،3-diphosphoglycerate بسلاسل بيتا لضغطها وتقليل تقارب الهيموجلوبين للأكسجين.
يحدث ارتباط 2،3 DPG بالهيموجلوبين عندما يكون في صورة غير مؤكسجة ، بينما يذوب في الرئة عن طريق ارتباط الهيموغلوبين بالأكسجين. في الواقع ، عندما يصل الهيموجلوبين إلى الأنسجة ، فإن سلاسل β هم أول من أطلق الأكسجين وهذا الفقد ينطوي على إزاحة المونومرات من المركز. بمجرد فتح التجويف الداخلي للماء ، يدخل DPG ويربط مع رباعي القطب مكونًا روابط غير متجانسة بين مجموعاته سالبة الشحنة والليسين والهيستيدين بقايا السلاسل بيتا ، موجبة الشحنة.يمكن للبنية المستقرة أيضًا إطلاق الأكسجين من سلسلتي α. ومع ذلك ، تحدث العملية العكسية في الرئتين ؛ عند ضغط الأكسجين المرتفع ، تكون سلاسل α هي أول من تربطها ويتم "ضغط" DPG وطرده من رباعي الأسطوانات ، مما يسمح بربط سلسلة أكسجين أسهل.
لا يمكن أن يرتبط 2،3 بيسفوسفوغليسيرات بالهيموجلوبين الجنيني ، لأن هذا الجزيء يخلو من السلاسل B التي يرتبط بها 2،3 DPG. وهذا يفسر الانجذاب الأكبر للأكسجين للهيموجلوبين الجنيني من الهيموجلوبين الأمومي ، وهي خاصية تسمح بدم الجنين استخراج الأكسجين من دم الأم.