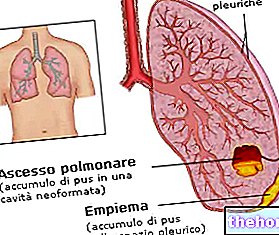
المكونات النشطة: كوليستين (كوليستيميثات الصوديوم)
كوليمايسين 1،000،000 IU / 4ml مسحوق ومذيب لمحلول الحقن أو التسريب
لماذا يستخدم Colimycin؟ لما هذا؟
يحتوي كوليمايسين على كوليستيميثات الصوديوم.
يُعطى الكوليمايسين عن طريق الحقن لعلاج بعض أنواع العدوى الشديدة التي تسببها بكتيريا معينة. يستخدم كوليمايسين عندما لا تكون المضادات الحيوية الأخرى مناسبة.
موانع الاستعمال عندما لا ينبغي استخدام كوليمايسين
لا تستخدم كوليمايسين
- إذا كنت تعاني من حساسية (شديدة الحساسية) من كوليستيميثات الصوديوم أو كوليستين أو بوليميكسينات أخرى ؛
- إذا كنت حاملاً (أنظري قسم "الحمل والرضاعة") ؛
- إذا كنت في فترة الرضاعة (أنظري قسم "الحمل والرضاعة") ؛
احتياطات الاستخدام ما تحتاج إلى معرفته قبل تناول كوليمايسين
تحدث إلى طبيبك أو الصيدلي أو الممرضة قبل استخدام كوليمايسين:
- إذا كان لديك أو كان لديك مشاكل في الكلى.
- إذا كنت تعاني من الوهن العضلي الشديد
- إذا كنت تعاني من البورفيريا.
في الأطفال الخدج وحديثي الولادة ، يجب توخي الحذر عند استخدام Colimycin ، لأن الكلى لم تتطور بشكل كامل بعد.
التفاعلات أي الأدوية أو الأطعمة يمكن أن تعدل من تأثير كوليميسين
أخبر طبيبك أو الصيدلي إذا كنت تتناول أو تناولت مؤخرًا أو قد تتناول أي أدوية أخرى.
من المهم بشكل خاص أن تتصل بطبيبك إذا كنت:
- الأدوية التي يمكن أن تؤثر على وظائف الكلى. إذا كنت تتناول هذا النوع من الأدوية في نفس الوقت مع كوليمايسين ، فقد يزداد خطر تلف الكلى.
- الأدوية التي يمكن أن تؤثر على الجهاز العصبي. إذا كنت تتناول هذا النوع من الأدوية في نفس الوقت مع كوليمايسين ، فقد يزداد خطر الآثار الجانبية التي تؤثر على الجهاز العصبي.
- أدوية تسمى مرخيات العضلات ، وغالبًا ما تستخدم أثناء التخدير العام ، وقد يعزز كوليمايسين من تأثير هذه الأدوية ، إذا تم إعطاؤك مخدرًا عامًا ، فيرجى إخبار طبيب التخدير عن استخدامك لكوليمايسين.
إذا كنت تعاني من الوهن العضلي الوبيل وتتناول أيضًا مضادات حيوية أخرى تسمى الماكروليدات (مثل أزيثروميسين أو كلاريثروميسين أو إريثروميسين) أو مضادات حيوية تسمى الفلوروكينولونات (مثل أوفلوكساسين ونورفلوكساسين وسيبروفلوكساسين) ، فإن تناول الكوليمايسين يزيد من خطر ضعف العضلات وصعوبة التنفس.
إذا تلقيت كوليستيميثات الصوديوم في نفس الوقت عن طريق التسريب والاستنشاق ، فقد تزداد مخاطر الآثار الجانبية.
تحذيرات من المهم معرفة ما يلي:
الحمل والرضاعة
إذا كنت حاملاً أو مرضعة ، تعتقدين أنك حامل أو تخططين لإنجاب طفل ، اسألي طبيبك للحصول على المشورة قبل استخدام هذا الدواء.
يجب عدم استخدام كوليميسين أثناء الحمل أو إذا كنت مرضعة (انظر قسم "لا تستخدم كوليميسين").
السياقة واستعمال الماكنات
أثناء العلاج بكوليمايسين ، قد تحدث اضطرابات في الجهاز العصبي مثل وخز حول الفم ، وخز في الأطراف ، وحكة ودوخة. إذا حدث هذا ، فلا تقود ولا تستخدم أي أدوات أو آلات.
الجرعة وطريقة ووقت الإعطاء كيفية استخدام كوليمايسين: الجرعات
يُعطى طبيبك Colimycin على شكل تسريب في الوريد لمدة 30 إلى 60 دقيقة.
في علاج الالتهابات البكتيرية ، من المهم إكمال دورة العلاج بأكملها ، وسيقرر طبيبك كيف ومدة إعطائك كوليمايسين.
الجرعة اليومية المعتادة للبالغين 9 ملايين وحدة مقسمة إلى جرعتين أو ثلاث جرعات. إذا كنت مريضًا جدًا ، فسيتم إعطاؤك جرعة تزيد عن 9 ملايين وحدة مرة واحدة في بداية العلاج.
في بعض الحالات ، قد يقرر طبيبك أن يعطيك جرعة يومية أعلى ، بحد أقصى 12 مليون وحدة.
الجرعة اليومية المعتادة للأطفال الذين يصل وزنهم إلى 40 كجم هي 75.000-150.000 وحدة لكل كيلوجرام من وزن الجسم ، مقسمة إلى ثلاث جرعات.
أحيانًا يتم إعطاء جرعات أعلى في حالات التليف الكيسي.
عادةً ما يتلقى الأطفال والبالغون الذين يعانون من مشاكل في الكلى ، حتى عند غسيل الكلى ، جرعات أقل. سيقوم طبيبك بفحص وظائف الكلى بانتظام أثناء تلقيك Colimycin.
الجرعة الزائدة ماذا تفعل إذا تناولت جرعة زائدة من كوليميسين
إذا كنت تستخدم المزيد من كوليمايسين أكثر مما ينبغي
نظرًا لأن الطبيب سيعطيك كوليمايسين ، فمن غير المحتمل أن يتم إعطاؤك جرعة غير صحيحة. إذا كان لديك أي أسئلة حول كمية هذا الدواء التي يجب أن تعطى لك ، اسأل طبيبك أو ممرضتك.تشمل أعراض تناول الكثير من الكوليمايسين:
- الخمول (النعاس).
- الارتباك (اضطراب عقلي).
- الذهان (تغيير حاد في التوازن النفسي) ؛
- - الدوخة (الشعور بعدم الثبات).
- ترنح (عدم القدرة على الوقوف منتصبا) ؛
- تنمل الوجه (حساسية متغيرة في الوجه) ؛
- رأرأة (حركات العين السريعة وغير المنضبط) ؛
- صعوبة في الكلام
- اضطرابات الكلى الحادة مثل الانخفاض الحاد في حجم البول وزيادة النيتروجين والكرياتينين في الدم.
- ضعف العضلات
- انقطاع النفس (صعوبة في التنفس).
إذا نسيت استخدام كوليمايسين
إذا كنت تعتقد أنك نسيت جرعة من كوليمايسين ، من فضلك أخبر طبيبك أو الصيدلي أو الممرضة.
إذا توقفت عن استخدام كوليمايسين
سيقرر طبيبك المدة التي ستحصل فيها على كوليمايسين. من المهم أن تكمل علاجك على النحو الذي أوصى به طبيبك ، وإلا فقد تزداد الأعراض سوءًا.
إذا كان لديك أي أسئلة أخرى حول استخدام هذا الدواء ، اسأل طبيبك أو الصيدلي أو الممرضة.
الآثار الجانبية ما هي الآثار الجانبية للكوليمايسين
مثل جميع الأدوية ، يمكن أن يسبب هذا الدواء آثارًا جانبية ، على الرغم من عدم حدوثها لدى الجميع.
بعض الآثار الجانبية يمكن أن تكون خطيرة
أخبر طبيبك أو ممرضتك على الفور إذا لاحظت أيًا من الأعراض التالية:
- أزيز أو صعوبة في التنفس يمكن أن تؤدي إلى انهيار أو طفح جلدي أو حكة أو خلايا على الجلد. يمكن أن تكون هذه علامات لرد فعل تحسسي شديد.
- إسهال. يمكن أن يكون من أعراض التهاب الأمعاء الحاد.
تم الإبلاغ أيضًا عن الآثار الجانبية التالية:
- تفاعل موقع الحقن
- مشاكل الكلى مثل الفشل الكلوي ، التسمم الكلوي ، زيادة النيتروجين والكرياتينين في الدم ، انخفاض حجم البول.هذه التأثيرات أكثر احتمالا في المرضى الذين يعانون بالفعل من ضعف وظائف الكلى أو الذين يتناولون كوليمايسين في نفس الوقت مع الأدوية الأخرى التي تؤثر على الكلى أو جرعة عالية جدًا ، وعادة ما تتحسن هذه المشاكل عند التوقف عن العلاج أو تقليل جرعة الكوليمايسين.
- مشاكل عصبية مثل عدم القدرة على التنفس بسبب شلل عضلات الصدر ، التنميل أو الوخز (خاصة حول الوجه) ، الدوخة أو فقدان التوازن ، تغيرات في ضغط الدم أو تدفق الدم (والتي تشمل الضعف والحرارة الشديدة) ، صعوبة الكلام. من المرجح أن تحدث الآثار الجانبية التي تؤثر على الجهاز العصبي عندما تكون جرعة الكوليمايسين عالية جدًا ، في الأشخاص الذين يعانون من ضعف في وظائف الكلى أو في أولئك الذين يتلقون أيضًا أدوية استرخاء العضلات أو الأدوية الأخرى التي لها تأثير مماثل من خلال التأثير على الجهاز العصبي. النظام.
- الارتباك والمشاكل العقلية (بما في ذلك فقدان الإحساس بالواقع)
- مشاكل بصرية
- دوار
- حمى.
- اضطرابات الجهاز الهضمي: الإسهال.
التبليغ عن الأعراض الجانبية
إذا ظهرت عليك أي آثار جانبية ، تحدث إلى طبيبك أو الصيدلي أو الممرضة ، وهذا يشمل أي آثار جانبية محتملة غير مدرجة في هذه النشرة.يمكنك أيضًا الإبلاغ عن الآثار الجانبية مباشرة.: https://www.aifa.gov.it/content / segnalazioni-reazioni-avverse
من خلال الإبلاغ عن الآثار الجانبية ، يمكنك المساعدة في توفير مزيد من المعلومات حول سلامة هذا الدواء.
انتهاء الصلاحية والاحتفاظ
احفظ هذا الدواء بعيدًا عن رؤية ومتناول أيدي الأطفال.
لا تستخدم هذا الدواء بعد تاريخ انتهاء الصلاحية المدون على العبوة الكرتونية والزجاجة بعد: EXP يشير تاريخ انتهاء الصلاحية إلى اليوم الأخير من ذلك الشهر.
لا تخزن فوق 25 درجة مئوية.
يجب إذابة المسحوق الموجود في القارورة فقط في وقت الاستخدام مع المحلول الفسيولوجي الموجود في القارورة المتوفرة داخل العبوة.
خلال هذه العملية ، من الممكن إدراك الاختلافات في الضغط الذي يجب أن يمارس على مكبس المحقنة لإدخال المذيب في القارورة مع المسحوق. هذه الاختلافات ، التي يمكن ملاحظتها بين عبوات مختلفة من الكوليمايسين ، ليست في حد ذاتها مؤشرًا على وجود خلل في جودة الدواء.
كل قنينة معاد تكوينها من محلول Colimycin للحقن أو التسريب هي للاستخدام الفردي فقط. يجب التخلص من أي محلول متبقي غير مستخدم (استخدام مرة واحدة).
بعد إعادة التكوين ، يجب استخدام Colimycin على الفور.
يجب استخدام المحلول المعاد تكوينه فقط إذا كان واضحًا وخاليًا من الجزيئات.
لا تقم بإلقاء أي أدوية في مياه الصرف الصحي أو النفايات المنزلية ، اسأل الصيدلي عن كيفية التخلص من الأدوية التي لم تعد تستخدمها ، فهذا سيساعد في حماية البيئة.
ما يحتويه كوليمايسين
- العنصر النشط هو كوليستيميثات الصوديوم
- المكونات الأخرى الموجودة في أمبولة المذيب هي كلوريد الصوديوم والماء للحقن.
كيف يبدو كوليميسين وما هي محتويات العبوة
يوجد في كل عبوة من Colimycin قنينة تحتوي على المادة الفعالة في مسحوق ، وقنينة تحتوي على مذيب (محلول كلوريد الصوديوم الفسيولوجي وماء للحقن).
مسحوق الكوليميسين أبيض. المذيب هو محلول واضح وعديم اللون.
نشرة حزمة المصدر: AIFA (وكالة الأدوية الإيطالية). تم نشر المحتوى في يناير 2016. المعلومات الموجودة قد لا تكون محدثة.
للوصول إلى أحدث إصدار ، يُنصح بالوصول إلى موقع AIFA (وكالة الأدوية الإيطالية). إخلاء المسؤولية والمعلومات المفيدة.
01.0 اسم المنتج الطبي
كوليميسين 1.000.000 IU / 4 مل بودرة ومذيب لمحلول الحقن أو التسريب
02.0 التركيب النوعي والكمي
تحتوي كل قنينة على: كوليستيميثات الصوديوم 1،000،000 وحدة دولية.
للحصول على قائمة كاملة من السواغات ، انظر القسم 6.1.
03.0 الشكل الصيدلاني
مسحوق ومذيب لمحلول الحقن أو التسريب.
04.0 المعلومات السريرية
04.1 المؤشرات العلاجية
يشار إلى الكوليمايسين في البالغين والأطفال ، بما في ذلك حديثي الولادة ، لعلاج الالتهابات الخطيرة بسبب بعض مسببات الأمراض سالبة الجرام في المرضى الذين تكون خيارات العلاج لهم محدودة (انظر الأقسام 4.2 و 4.4 و 4.8 و 5.1).
انتبه إلى الإرشادات الرسمية للاستخدام الصحيح للعوامل المضادة للبكتيريا.
04.2 الجرعة وطريقة الإدارة
يجب تحديد الجرعة ومدة العلاج مع مراعاة شدة الإصابة والاستجابة السريرية ، ويجب اتباع الإرشادات العلاجية.
يتم التعبير عن الجرعة بوحدات دولية (IU) من كوليستيميثات الصوديوم (CMS). يوجد في نهاية الفقرة جدول تحويل من IU إلى mg من CMS وإلى mg من النشاط الأساسي للكوليستين (نشاط قاعدة كوليستين، CBA).
الجرعة
تستند توصيات الجرعات التالية إلى بيانات حركية دوائية محدودة للسكان في المرضى ذوي الحالات الحرجة (انظر القسم 4.4):
الكبار والمراهقون
جرعة الصيانة: 9 MIU / يوم مقسمة إلى 2-3 جرعات.
في المرضى ذوي الحالات الحرجة ، يجب إعطاء جرعة تحميل من 9 MIU.
لم يتم تحديد الفاصل الزمني الأنسب لجرعة الصيانة الأولى.
تشير النماذج إلى أن جرعات التحميل والصيانة التي تصل إلى 12 MIU قد تكون مطلوبة في المرضى الذين يعانون من وظائف الكلى الجيدة في بعض الحالات. ومع ذلك ، فإن التجربة السريرية مع هذه الجرعات محدودة للغاية ولم يتم التأكد من سلامتها.
جرعة التحميل صالحة للمرضى الذين يعانون من وظائف الكلى الطبيعية أو المنخفضة ، بما في ذلك أولئك الذين يخضعون لعلاج استبدال الكلى.
القصور الكلوي
يجب تعديل الجرعة في حالة وجود اختلال كلوي ، لكن بيانات الحرائك الدوائية المتاحة للمرضى الذين يعانون من اختلال وظائف الكلى محدودة للغاية.
يتم توفير تعديلات الجرعة التالية للإرشاد.
ينصح بتخفيض الجرعة عند المرضى الذين يعانون من تصفية الكرياتينين
يوصى بإدارتين يوميًا.
MIU = مليون وحدة دولية
غسيل الكلى وترشيح الدم المستمر
يبدو كوليستين قابلاً للتبديل بالطرق التقليدية لغسيل الكلى والترشيح المستمر الوريدي الهيمو (ديا) (ترشيح الدم الوريدي المستمر (ضياء)، CVVHF ، CVVHDF). تتوفر بيانات محدودة للغاية من دراسات الحرائك الدوائية السكانية في أعداد صغيرة جدًا من المرضى الذين يخضعون للعلاج بالبدائل الكلوية. لا يمكن تقديم توصيات محددة للجرعة. يمكن النظر في الأنظمة العلاجية التالية.
غسيل الكلى
عدد الأيام بدون غسيل الكلى: 2.25 MIU / يوم (2.2-2.3 MIU / يوم).
أيام غسيل الكلى: 3 MIU / يوم في أيام غسيل الكلى ، على أن يتم تناولها بعد جلسة غسيل الكلى.
يوصى بإدارتين يوميًا.
CVVHF / CVVHDF
كما هو الحال في المرضى الذين يعانون من وظائف الكلى الطبيعية. يوصى بثلاث إدارات يومية.
اختلال كبدي
لا توجد بيانات متاحة في مرضى القصور الكبدي. ينصح بالحذر عند إعطاء كوليستيميثات الصوديوم لهؤلاء المرضى.
المواطنين من كبار السن
لا تعتبر تعديلات الجرعة ضرورية في المرضى المسنين الذين يعانون من وظائف الكلى الطبيعية.
سكان الأطفال
البيانات لدعم نظام الجرعات في مرضى الأطفال محدودة للغاية. يجب أن يؤخذ النضج الكلوي في الاعتبار لتحديد الجرعة. يجب أن تعتمد الجرعة على وزن كتلة الجسم النحيل.
الأطفال ≤40 كجم
75.000-150.000 وحدة دولية / كجم / يوم مقسمة على 3 جرعات.
بالنسبة للأطفال الذين يزيد وزنهم عن 40 كجم ، يجب مراعاة توصيات الجرعة الصالحة للبالغين.
تم الإبلاغ عن استخدام جرعات أكبر من 150000 وحدة دولية / كجم / يوم في الأطفال المصابين بالتليف الكيسي.
لا توجد بيانات متاحة حول استخدام أو مدى جرعات التحميل في الأطفال المصابين بأمراض خطيرة.
لم يتم تقديم توصيات بشأن الجرعات عند الأطفال الذين يعانون من اختلال وظائف الكلى.
الإدارة داخل القراب وداخل البطينات
بناءً على البيانات المحدودة ، يوصى بالجرعة التالية للبالغين:
طريق داخل البطينات
125000 وحدة دولية / يوم
يجب ألا تتجاوز الجرعات المعطاة داخل القراب تلك الموصى بها للاستخدام داخل البطين.
لا يمكن تقديم توصيات جرعة محددة لطرق الإعطاء داخل القراب وداخل البطينات عند الأطفال.
طريقة الإعطاء
إدارة الكوليميسين عن طريق الوريد عن طريق التسريب البطيء لمدة 30-60 دقيقة.
في محلول مائي ، يتحلل كوليستيميثات الصوديوم إلى المادة الفعالة كوليستين. لتحضير الجرعة ، خاصةً عندما تتكون من محتويات عدة قوارير ، يجب إعادة تكوين الجرعة المطلوبة في ظروف التعقيم المطلق (انظر القسم 6.6).
طاولة الحوار
في الاتحاد الأوروبي ، يجب وصف جرعة كوليستيميتات الصوديوم (CMS) وإدارتها فقط بوحدات دولية (IU) ، ويُظهر الملصق عدد IU لكل قارورة.
في الماضي كان هناك ارتباك وأخطاء في الإدارة بسبب استخدام وحدات مختلفة لقياس الجرعة من حيث الفاعلية.في الولايات المتحدة وأجزاء أخرى من العالم ، يتم التعبير عن الجرعة بالملليغرام من النشاط الأساسي للكوليستين (ملليغرام من نشاط قاعدة كوليستين، mg CBA).
جدول التحويل التالي معطى كدليل والقيم تعتبر اسمية وتقريبية فقط.
جدول تحويل CMS
* الفعالية الاسمية للمادة الدوائية = 12500 وحدة دولية / مجم
04.3 موانع الاستعمال
فرط الحساسية للكوليستين والمضادات الحيوية الأخرى من عائلة البوليميكسين أو لأحد السواغات المدرجة في القسم 6.1.
الحمل والرضاعة (انظر القسم 4.6).
04.4 تحذيرات خاصة واحتياطات مناسبة للاستخدام
كلما كان ذلك ممكنًا ، ينبغي النظر في الإعطاء المشترك لكوليستيميثات الصوديوم في الوريد مع عامل مضاد للبكتيريا آخر ، مع الأخذ في الاعتبار الحساسية المتبقية لمسببات الأمراض أو مسببات الأمراض التي يتم علاجها. نظرًا لأنه تم الإبلاغ عن تطور مقاومة للكوليستين في الوريد ، خاصة عند استخدامه بمفرده ، يجب أيضًا مراعاة الإعطاء المشترك مع مضادات الجراثيم الأخرى لمنع تطور المقاومة.
تتوفر فقط بيانات سريرية محدودة حول فعالية وسلامة كوليستيميثات الصوديوم الذي يتم إعطاؤه عن طريق الوريد.تستند الجرعات الموصى بها في جميع المجموعات السكانية الفرعية أيضًا إلى بيانات محدودة (سريرية وحركية دوائية / ديناميكية دوائية). على وجه الخصوص ، تتوفر بيانات السلامة. محدودة لاستخدام الجرعات العالية (> 6 MIU / يوم) ، لاستخدام جرعة التحميل وللفئات الخاصة (مرضى القصور الكلوي والأطفال) يجب استخدام كوليستيميثات الصوديوم فقط عندما تكون المضادات الحيوية الأخرى الأكثر شيوعًا غير فعالة أو غير مناسبة.
يجب إجراء مراقبة وظائف الكلى في جميع المرضى في بداية العلاج وعلى فترات منتظمة أثناء العلاج.يجب تعديل جرعة الصوديوم كوليستيميثات وفقًا لتصفية الكرياتينين (انظر القسم 4.2). زيادة خطر السمية الكلوية بسبب الكولستين (انظر القسمين 4.5 و 4.8). في بعض الدراسات ، ارتبطت السمية الكلوية بالجرعة التراكمية ومدة العلاج. .
يجب توخي الحذر عند إعطاء كوليستيميثات الصوديوم للرضع الذين تقل أعمارهم عن سنة واحدة ، حيث أن وظائف الكلى لم تصل إلى مرحلة النضج الكامل في هذه الفئة العمرية ، وعلاوة على ذلك ، فإن تأثير وظيفة الكلى والتمثيل الغذائي غير الناضجة غير معروف. لكوليستين.
في حالة حدوث رد فعل تحسسي ، يجب التوقف عن العلاج باستخدام كوليستيميثات الصوديوم واتخاذ التدابير المناسبة.
لوحظ أن التراكيز المرتفعة من كوليستيميثات الصوديوم في المصل ، والتي قد تكون ناجمة عن جرعة زائدة أو فقدان جرعة في المرضى الذين يعانون من اختلال كلوي ، تسبب تأثيرات سمية عصبية مثل تنمل الوجه ، ضعف العضلات ، الدوخة ، تداخل الكلام ، عدم الاستقرار الحركي الوعائي ، الاضطرابات البصرية ، الارتباك. والذهان وانقطاع النفس (انظر القسم 4.7). ستكون المساعدة التنفسية مطلوبة حتى تنخفض مستويات الدم. ويمكن استئناف العلاج ، إذا كان هناك حالة مهددة للحياة للمريض ، بجرعات أقل. قد لا تظهر الأعراض الذاتية التي أبلغ عنها الكبار في الأطفال. أصغر ، لذلك هم يجب مراقبة وظائف الكلى.
يجب مراقبة المرضى من أجل التنميل حول الفم وتنمل الأطراف وهي علامات على الجرعة الزائدة (انظر القسم 4.9).
من المعروف أن كوليستيميثات الصوديوم يقلل من إطلاق الأسيتيل كولين قبل المشبكي عند التقاطع العصبي العضلي ويجب استخدامه بحذر شديد وفقط إذا لزم الأمر بشكل واضح في المرضى الذين يعانون من الوهن العضلي الشديد.
تم الإبلاغ عن حالات توقف التنفس بعد إعطاء العضل لكوليستيميثات الصوديوم. يؤدي اختلال وظائف الكلى إلى زيادة احتمالية الإصابة بانقطاع النفس والحصار العصبي العضلي بعد تناول كوليستيميثات الصوديوم.
يجب استخدام كوليستيميثات الصوديوم بحذر شديد عند مرضى البورفيريا.
تم الإبلاغ عن التهاب القولون المرتبط بالمضادات الحيوية والتهاب القولون الغشائي الكاذب مع جميع مضادات الجراثيم تقريبًا ويمكن أن يحدث أيضًا مع كوليستيميثات الصوديوم. يمكن أن تتراوح شدتها من خفيفة إلى مهددة للحياة. من المهم أن يؤخذ هذا التشخيص في الاعتبار عند المرضى الذين يصابون بالإسهال أثناء أو بعد استخدام كوليستيميثات الصوديوم (انظر القسم 4.8) ، وينبغي النظر في وقف العلاج وبدء علاج محدد. المطثية العسيرة. لا ينبغي إعطاء المنتجات الطبية التي تمنع التمعج.
لا يعبر كوليستيميثات الصوديوم الذي يتم تناوله عن طريق الوريد حاجز الدم في الدماغ إلى حد ذي صلة سريريًا. لم يتم تقييم الإدارة داخل القراب أو داخل البطينات لكوليستيميثات الصوديوم في علاج التهاب السحايا بشكل منهجي في الدراسات السريرية ولا يتم دعمها إلا من خلال تقارير الحالة الفردية. البيانات لدعم علم الوجود محدودة للغاية. كان التأثير الضار الأكثر شيوعًا بعد إعطاء CMS هو التهاب السحايا العقيم (انظر القسم 4.8).
أثناء العلاج الجهازي ، يوصى بمراقبة تركيزات البلازما عند الولدان والمرضى الذين يعانون من القصور الكلوي والمصابين بالتليف الكيسي.
04.5 التفاعلات مع المنتجات الطبية الأخرى وأشكال التفاعل الأخرى
في حالة الاستخدام المتزامن لكوليستيميثات الصوديوم في الوريد مع المنتجات الطبية الأخرى التي قد تكون سامة كلوية أو عصبية (على سبيل المثال ، المضادات الحيوية التالية: كاناميسين ، نيومايسين ، ستربتومايسين ، جنتاميسين ، توبراميسين) يجب توخي الحذر الشديد.
تم الإبلاغ عن بعض المضادات الحيوية ، مثل aminoglycosides و polymyxins الأخرى ، تتداخل مع انتقال العصب عند الموصل العصبي العضلي.
لا يمكن إعطاء الأمينوغليكوزيدات والبوليميكسين مع الكوليمايسين عن طريق الحقن إلا تحت إشراف طبي صارم.
يجب توخي الحذر في حالة الاستخدام المتزامن مع الأشكال الصيدلانية الأخرى من كوليستيميثات الصوديوم ، حيث أن الخبرة محدودة وهناك خطر السمية التراكمية.
لم يتم إجراء دراسات تفاعل في الجسم الحي. لم يتم تمييز آلية تحويل كوليستيميثات الصوديوم إلى العنصر النشط كوليستين. آلية إزالة الكوليستين ، بما في ذلك العمليات الكلوية ، غير معروفة أيضًا. لم يسبب أي من كوليستيميثات الصوديوم ولا كوليستين نشاط أي من إنزيمات P450 (CYP) التي تم اختبارها (CYP1A2 ، 2B6 ، 2C8 ، 2C9 ، 2C19 و 3A4 / 5) في الدراسات في المختبر على خلايا الكبد البشرية.
يجب أن تؤخذ التفاعلات الدوائية المحتملة في الاعتبار عند المشاركة في إدارة Colimycin مع المنتجات الطبية المعروفة بتثبيط أو تحفيز الإنزيمات المسؤولة عن استقلاب الدواء أو التي هي ركائز آليات النقل الكلوي.
نظرًا لتأثيرات الكوليستين على إطلاق الأسيتيل كولين ، يجب استخدام مرخيات العضلات غير المزيلة للاستقطاب بحذر عند المرضى الذين يتلقون كوليستيميثات الصوديوم ، حيث قد تطول آثارهم (انظر القسم 4.4).
يجب إجراء العلاج المتزامن مع كوليستيميتات الصوديوم والماكروليدات مثل أزيثروميسين وكلاريثروميسين أو الفلوروكينولونات مثل النورفلوكساسين وسيبروفلوكساسين بحذر عند مرضى الوهن العضلي الشديد (انظر القسم 4.4).
04.6 الحمل والرضاعة
يمنع استخدام الدواء في حالة الحمل وأثناء الإرضاع (انظر القسم 4.3).
في الثلث الثاني والثالث من الحمل ، هناك خطر حدوث تسمم جنيني محتمل ، حيث يوجد كوليستين في الحليب ولكن يتم امتصاصه بشكل سيئ من الأمعاء.
04.7 التأثيرات على القدرة على السياقة واستعمال الآلات
قد تحدث الاضطرابات العصبية أثناء العلاج (انظر القسم 4.4). يجب نصح المرضى بعدم القيادة أو استخدام الآلات في حالة حدوث هذه الآثار.
04.8 الآثار غير المرغوب فيها
تم الإبلاغ عن ردود الفعل السلبية التالية:
اضطرابات الجهاز المناعي: تفاعلات فرط الحساسية مثل الطفح الجلدي والوذمة الوعائية.
اضطرابات نفسية: الارتباك والذهان.
اضطرابات الجهاز العصبي: تأثيرات سامة للأعصاب ، تنمل ، دوار ، وخز في الأطراف واللسان ، نادرا اضطراب الكلام واختلال في الجهاز العصبي اللاإرادي. إحصار عصبي عضلي في حالة الجرعة الزائدة أو المشاركة مع العوامل العلاجية أو في حالة عدم كفاية التخلص الكلوي.
اضطرابات العين: اضطرابات بصرية.
اضطرابات الأذن والمتاهة: دوار.
اضطرابات الجهاز التنفسي والصدر والمنصف: ضيق التنفس حتى القصور، انقطاع النفس.
اضطرابات الجهاز الهضمي: إسهال (أنظر القسم 4.4).
اضطرابات الجلد والأنسجة تحت الجلد: حكة معممة ، شرى ، طفح جلدي.
اضطرابات الكلى والمسالك البولية: فشل كلوي ، اختلال كلوي يظهر من خلال زيادة الكرياتينين و / أو اليوريا في الدم و / أو انخفاض التصفية الكلوية للكرياتينين.
الاضطرابات العامة وظروف الموقع الإدارة: حمى ، تفاعل في موضع الحقن.
الاختبارات التشخيصية: انخفاض إنتاج البول ، انخفاض تصفية الكرياتينين.
الإبلاغ عن ردود الفعل السلبية المشتبه بها
يعد الإبلاغ عن التفاعلات العكسية المشتبه بها التي تحدث بعد الحصول على ترخيص من المنتج الطبي أمرًا مهمًا لأنه يسمح بالمراقبة المستمرة لتوازن الفوائد / المخاطر للمنتج الطبي. يُطلب من المتخصصين في الرعاية الصحية الإبلاغ عن أي ردود فعل سلبية مشتبه بها عبر نظام الإبلاغ الوطني. "وكالة الأدوية الإيطالية ، الموقع الإلكتروني: www.agenziafarmaco.gov.it/it/responsabili.
04.9 جرعة زائدة
يمكن ملاحظة أعراض الجرعة الزائدة في المرضى الذين يعانون من اختلال وظائف الكلى. الجرعات التي تزيد عن الحد الأقصى يمكن أن تسبب فشل كلوي حاد يتجلى في قلة البول ، آزوتيميا ، فرط كرياتين الدم ، وعادة ما يمكن عكسه عن طريق التوقف عن العلاج.
لوحظ أن التراكيز المرتفعة من كوليستيميثات الصوديوم في الدم ، والتي قد تكون ناجمة عن جرعة زائدة أو نقصان في الجرعة المفقودة لدى مرضى القصور الكلوي ، تسبب تأثيرات سمية عصبية مثل الخمول ، ترنح ، تنمل الوجه ، ضعف العضلات ، الدوخة ، صعوبة الكلام ، عدم الاستقرار الحركي الوعائي ، اضطرابات بصرية ، ارتباك ، ذهان.
يمكن أن يحدث انقطاع النفس أيضًا نتيجة لتوقف الجهاز التنفسي والوفاة.
يجب مراقبة المرضى من أجل التنميل حول الفم وتنمل الأطراف والتي هي علامات على جرعة زائدة (انظر القسم 4.4). في حالة الجرعة الزائدة ، يجب التوقف عن العلاج باستخدام كوليستيميثات الصوديوم واستخدام التدابير الداعمة المناسبة.
لا يتم التخلص من كوليستين عن طريق غسيل الكلى.
من غير المعروف ما إذا كان يمكن إزالة كوليستيميثات الصوديوم عن طريق غسيل الكلى أو غسيل الكلى البريتوني في حالات الجرعة الزائدة.
05.0 الخصائص الصيدلانية
05.1 الخصائص الديناميكية الدوائية
مجموعة العلاج الدوائي: مضادات الجراثيم للاستخدام الجهازي ، ومضادات الجراثيم الأخرى ، والبوليميكسين.
كود ATC: J01XB01.
آلية العمل
كوليستين هو مضاد جرثومي دوري متعدد الببتيد ينتمي إلى مجموعة البوليميكسين. يعتمد عمل البوليميكسين على الأضرار التي لحقت بغشاء الخلية والتأثيرات الفسيولوجية المترتبة على ذلك تكون قاتلة للبكتيريا.
المقاومة
تتميز البكتيريا المقاومة بتعديلات على مجموعات الفوسفات في عديدات السكاريد الدهنية والتي يتم استبدالها بالإيثانول أمين أو أمين أرابينوز. البكتيريا سالبة الجرام المقاومة بشكل طبيعي ، مثل المتقلبة الرائعة و بوركولديريا سيباسيا، إظهار الاستبدال الكامل للفوسفات الدهني بالإيثانولامين أو amino-arabinose.
من المتوقع حدوث مقاومة متصالبة بين كوليستين (بوليميكسين إي) وبوليميكسين ب. نظرًا لأن آلية عمل بوليميكسين مختلفة عن تلك الخاصة بمضادات الجراثيم الأخرى ، فإن مقاومة الكوليستين والبوليميكسين بسبب الآلية الموضحة أعلاه وحدها لا ينبغي أن تحفز المقاومة ضد الفئات الأخرى المخدرات.
الارتباط الدوائي / الديناميكي الدوائي
وقد لوحظ أن البوليميكسين يظهر تأثير مبيد للجراثيم يعتمد على التركيز على البكتيريا الحساسة. يعتقد أن FAUC / MIC لهما علاقة بالفعالية السريرية.
تركيزات حد EUCAST
إلى التركيزات المحددة صالحة لجرعة 2-3 MIU x 3. قد تكون هناك حاجة لجرعة التحميل (9 MIU).
حساسية
قد يختلف انتشار المقاومة المكتسبة جغرافياً وبمرور الوقت بالنسبة لأنواع معينة ومن المستحسن الحصول على معلومات محلية عن المقاومة ، خاصة لعلاج العدوى الشديدة. عند الضرورة ، يجب التماس مشورة الخبراء عندما يكون الانتشار المحلي للمقاومة بحيث تصبح فائدة المنتج الطبي ، على الأقل في بعض أنواع العدوى ، موضع شك.
05.2 "خصائص حركية الدواء
هناك معلومات محدودة عن الحرائك الدوائية لكوليستيميثات الصوديوم (CMS) والكوليستين. تشير بعض البيانات إلى أن الحرائك الدوائية في المرضى المصابين بأمراض خطيرة تختلف عن تلك التي لوحظت في المرضى الذين يعانون من اختلالات فسيولوجية أقل حدة وفي المتطوعين الأصحاء. تستند البيانات التالية إلى الدراسات التي أجريت باستخدام طريقة HPLC لتحديد تركيزات البلازما لـ CMS / colistin.
بعد تسريب كوليستيميثات الصوديوم ، يتم تحويل الدواء الأولي غير الفعال إلى المادة الفعالة كوليستين. لوحظت ذروة تركيزات كوليستين في البلازما مع تأخير أقصاه 7 ساعات بعد إعطاء كوليستيميثات الصوديوم في المرضى المصابين بأمراض خطيرة.
توزيع
حجم توزيع الكوليستين في المتطوعين الأصحاء منخفض ويتوافق تقريبًا مع السائل خارج الخلية. يزداد حجم التوزيع بشكل كبير في الموضوعات ذات الحالات الحرجة. يكون الارتباط بالبروتين معتدلاً وينخفض بتركيزات أعلى. في حالة عدم وجود التهاب السحايا ، يكون تغلغل السائل الدماغي النخاعي ضئيلًا ، ولكنه يزيد في وجود التهاب السحايا.
يعرض كل من CMS و colistin الحرائك الدوائية الخطية على نطاق الجرعة ذات الصلة سريريًا.
إزالة
تشير التقديرات إلى أن حوالي 30٪ من كوليستيميثات الصوديوم يتحول إلى كوليستين في الأشخاص الأصحاء. يعتمد تخليصه على تصفية الكرياتينين ويتم تحويل نسبة أعلى من CMS إلى كوليستين في حالة انخفاض وظائف الكلى. في المرضى الذين يعانون من ضعف شديد في وظائف الكلى (تصفية الكبيبات بتصفية الكرياتينين. في الأشخاص الأصحاء ، يتم إفراز 60٪ -70٪ من CMS دون تغيير في البول خلال 24 ساعة.
يتم تمييز التخلص من المادة الفعالة كوليستين جزئياً فقط. يتم إعادة امتصاص كوليستين على نطاق واسع في النبيبات الكلوية ويمكن التخلص منه عن طريق الأيض غير الكلوي وعن طريق الأيض الكلوي ، مع خطر التراكم في الكلى. يتم تقليل تصفية الكوليستين في حالة الكلى ضعف ، ربما بسبب "زيادة تحويل CMS."
يبلغ عمر النصف للكوليستين في الأشخاص الأصحاء وفي الأشخاص المصابين بالتليف الكيسي ، على التوالي ، حوالي 3 ساعات و 4 ساعات ، مع خلوص إجمالي يبلغ حوالي 3 لتر / ساعة. في المرضى المصابين بأمراض خطيرة ، يطول عمر النصف إلى حوالي 9 - 18 ساعة.
05.3 بيانات السلامة قبل السريرية
قد تكون التأثيرات السامة للكوليستين ناتجة عن كوليستيميثات الصوديوم ويتم التعبير عنها في شكل تلف أنبوبي. مع 3 مغ / كغ قد يكون هناك زيادة في ازوتيميا ؛ مع 2.5 مغ / كغ قد يكون هناك بيلة زلالية وبيلة دموية. ومع ذلك ، هذه الظواهر يمكن عكسها بعد التوقف عن العلاج.جرعات عالية وطويلة من كوليستيميثات الصوديوم في المرضى الذين يعانون من أمراض الكلى يمكن أن تسبب السمية العصبية والسمية الكلوية ، والتي يجب تقليل جرعاتها بشكل مناسب.
06.0 المعلومات الصيدلانية
06.1 السواغات
كلوريد الصوديوم والماء للحقن.
06.2 عدم التوافق
في حالة عدم وجود دراسات عدم التوافق ، يجب عدم خلط هذا المنتج الطبي مع المنتجات الطبية الأخرى.
06.3 فترة الصلاحية
3 سنوات في تغليف سليم.
06.4 احتياطات خاصة للتخزين
لا تخزن فوق 25 درجة مئوية.
06.5 طبيعة العبوة الفورية ومحتويات العبوة
قنينة زجاجية تحتوى على 1،000،000 وحدة دولية من كوليستيميثات الصوديوم + 1 قارورة مذيب 4 مل.
06.6 تعليمات الاستخدام والتداول
قم بإذابة المسحوق الموجود في القارورة فقط في وقت الاستخدام مع المحلول الفسيولوجي الموجود في القارورة. أثناء هذه العملية ، من الممكن إدراك الاختلافات في الضغط الذي يجب أن يمارس على مكبس المحقنة لإدخال المذيب في القارورة مع المسحوق.قد تلاحظ بين عبوات مختلفة من Colimycin ، فهي ليست في حد ذاتها مؤشرًا على وجود خلل في جودة الدواء.
بعد إعادة التركيب ، يجب تخفيف المحلول إلى حجم مناسب للتسريب لمدة 30-60 دقيقة بمحلول كلوريد الصوديوم 9 مجم / مل (0.9٪) للتسريب.
يجب فحص المحلول بصريًا بحثًا عن وجود جزيئات أو تغير في اللون قبل الإعطاء. يجب استخدام المحلول فقط إذا كان واضحًا وخاليًا من الجزيئات.
07.0 حامل ترخيص التسويق
يو سي بي فارما ش. - فيا فاريسينا ، 162-20156 ميلانو (إيطاليا).
08.0 رقم ترخيص التسويق
A.I.C. ن. 011297013
09.0 تاريخ أول تفويض أو تجديد التفويض
تاريخ أول ترخيص: 23 يونيو 1956
تاريخ آخر تجديد: يونيو 2010
10.0 تاريخ مراجعة النص
28 يوليو 2015