المكونات النشطة: أوندانسيترون
أقراص مغلفة بالفيلم Ondansetron Mylan Generics 4 ملغ
أقراص مغلفة بالفيلم Ondansetron Mylan Generics 8 ملغ
لماذا يتم استخدام Ondansetron - الأدوية الجنيسة؟ لما هذا؟
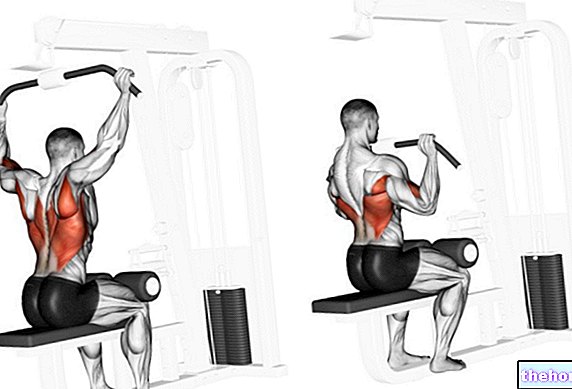
ينتمي Ondansetron Mylan Generics إلى مجموعة من الأدوية تسمى مضادات القيء أو الأدوية المضادة للقيء. يثبط أوندانسيترون تأثيرات الناقل العصبي السيروتونين في الدماغ ، ويسبب السيروتونين الغثيان والقيء.
يستخدم Ondansetron Mylan Generics في البالغين من أجل:
- السيطرة على الغثيان والقيء الناجم عن العلاج الكيميائي أو العلاج الإشعاعي للسرطان
- منع الغثيان والقيء بعد العملية
يستخدم Ondansetron Mylan Generics في الأطفال من أجل:
- السيطرة على الغثيان والقيء الناجم عن العلاج الكيميائي لدى الأطفال الذين تتراوح أعمارهم بين 6 أشهر وما فوق
- منع الغثيان والقيء بعد العملية في الأطفال الذين تتراوح أعمارهم بين شهر واحد وما فوق.
اسأل طبيبك أو ممرضتك أو الصيدلي إذا كنت ترغب في تفسيرات أخرى لهذه الاستخدامات.
موانع الاستعمال عندما لا ينبغي استخدام أوندانسيترون - الأدوية العامة
لا تأخذ Ondansetron Mylan Generics:
- إذا كان لديك حساسية من أوندانسيترون ، أو أي من المكونات الأخرى لهذا الدواء (المدرجة في القسم 6)
- إذا كنت تعاني من حساسية تجاه الأدوية الأخرى المضادة للقيء التي تنتمي إلى مجموعة مضادات مستقبلات السيروتونين الانتقائية (5-HT3) (مثل جرانيسيترون أو دولاسيترون) كما في هذه الحالات قد يكون لديك أيضًا حساسية من أوندانسيترون
- إذا كنت تتناول أبومورفين (يستخدم لعلاج مرض باركنسون).
إذا لم تكن متأكدًا ، تحدث إلى طبيبك أو ممرضتك أو الصيدلي قبل تناول Ondansetron Mylan Generics.
احتياطات الاستخدام ما تحتاج إلى معرفته قبل تناول جينريك أوندانسيترون
تحدث إلى طبيبك أو الصيدلي أو الممرضة قبل تناول Ondansetron Mylan Generics:
- إذا كنت تعاني من أي وقت مضى من مشاكل في القلب أو تغيرات في نظم القلب (عدم انتظام ضربات القلب أو اضطرابات التوصيل القلبي).
- إذا كنت تعاني من مشاكل في مستويات الأملاح في الدم مثل البوتاسيوم والصوديوم والمغنيسيوم
- إذا كنت تعاني من مشاكل معوية مثل انسداد معوي أو إذا كنت تعاني من إمساك شديد
- إذا كنت على وشك إزالة الزوائد الأنفية أو اللوزتين أو تم استئصالهما مؤخرًا ، لأن العلاج بهذا الدواء قد يخفي أعراض النزيف الداخلي
- إذا كنت طفلاً تقل مساحة سطح جسمك عن 0.6 م 2
- إذا كان لديك مشاكل في الكبد.
الأطفال والمراهقون
لا ينبغي إعطاء هذا الدواء للأطفال للوقاية من الغثيان والقيء بعد عملية المعدة.
إذا لم تكن متأكدًا مما إذا كان أي مما سبق ينطبق عليك ، فتحدث إلى طبيبك أو ممرضتك أو الصيدلي قبل تناول Ondansetron Mylan Generics.
التفاعلات: ما هي الأدوية أو الأطعمة التي قد تغير من تأثير أوندانسيترون - الأدوية الجنيسة
أخبر طبيبك أو ممرضتك أو الصيدلي إذا كنت تتناول أو تناولت مؤخرًا أو قد تتناول أي أدوية أخرى.وهذا يشمل أيضًا الأدوية التي تشتريها بدون وصفة طبية أو أدوية عشبية. وذلك لأن Ondansetron Mylan Generics يمكن أن يؤثر على الآخرين. قد تؤثر الأدوية أو الأدوية الأخرى تؤثر على Ondansetron Mylan Generics.
على وجه الخصوص ، أخبر طبيبك أو ممرضتك أو الصيدلي إذا كنت تتناول أيًا من الأدوية التالية:
- الأبومورفين (دواء يستخدم لعلاج مرض باركنسون) ، حيث تم الإبلاغ عن انخفاض كبير في ضغط الدم وفقدان الوعي عند استخدام الأبومورفين بالتزامن مع أوندانسيترون - فينيتوين أو كاربامازيبين (أدوية لعلاج الصرع) والتي يمكن أن تقلل من تأثير أوندانسيترون
- ريفامبيسين (مضاد حيوي يستخدم لعلاج الالتهابات مثل السل) والذي قد يقلل من آثار أوندانسيترون.
- المضادات الحيوية مثل الإريثروميسين أو الكيتوكونازول - الأدوية المضادة لاضطراب النظم مثل الأميودارون (تستخدم لعلاج عدم انتظام ضربات القلب)
- حاصرات بيتا مثل أتينولول أو تيمولول (تستخدم لعلاج بعض مشاكل القلب أو العين ، القلق أو لمنع الصداع النصفي) - ترامادول (مسكن للألم) يمكن تقليله بواسطة أوندانسيترون مايلان جينيركس
- أدوية للسرطان (خاصة الأنثراسيكلين والتراستوزوماب)
- بعض أنواع الأدوية المستخدمة لعلاج الاكتئاب المعروفة باسم SSRIs (مثبطات امتصاص السيروتونين الانتقائية) أو SNRIs (مثبطات امتصاص السيروتونين والنورابينفرين) ، حيث يمكن أن تسبب متلازمة السيروتونين ، وهو تفاعل قد يهدد الحياة إذا تم استخدامه بالاقتران مع أوندانسيترون. يمكن أن تشمل أعراض متلازمة السيروتونين مزيجًا مما يلي: الغثيان (الشعور بالغثيان) ، والتقيؤ ، والإثارة ، والإسهال ، وارتفاع درجة الحرارة ، وزيادة ضغط الدم ، والتعرق المفرط ، وسرعة ضربات القلب ، والهلوسة ، وفقدان التنسيق ، وردود الفعل المفرطة والغيبوبة.
إذا لم تكن متأكدًا مما إذا كان أي مما سبق ينطبق عليك ، فتحدث إلى طبيبك أو ممرضتك أو الصيدلي قبل تناول Ondansetron Mylan Generics.
تحذيرات من المهم معرفة ما يلي:
الحمل والرضاعة
لا ينصح باستخدام Ondansetron Mylan Generics أثناء الحمل.قبل تناول Ondansetron Mylan Generics ، اسأل طبيبك أو الصيدلي للحصول على المشورة إذا كنت حاملاً أو قد تصبحي حاملاً.
لا ترضع من الثدي أثناء العلاج باستخدام Ondansetron Mylan Generics. وذلك لأن هذا الدواء يمكن أن ينتقل إلى حليب الثدي. اسألي طبيبك أو الصيدلي أو القابلة للحصول على المشورة.
إذا كنت حاملاً أو مرضعة ، تعتقدين أنك حامل أو تخططين لإنجاب طفل ، اسألي طبيبك أو الصيدلي للحصول على المشورة قبل تناول هذا الدواء.
السياقة واستعمال الماكنات
لا يؤثر Ondansetron Mylan Generics على القدرة على القيادة أو استخدام الآلات.
يحتوي Ondansetron Mylan Generics على اللاكتوز
إذا أخبرك طبيبك أن لديك "عدم تحمل لبعض السكريات ، فاتصل بطبيبك قبل تناول هذا المنتج الطبي.
الجرعة وطريقة ووقت الإعطاء كيفية استخدام Ondansetron - الأدوية العامة: علم الجرعات
احرص دائمًا على تناول هذا الدواء تمامًا كما أخبرك طبيبك أو الصيدلي. اسأل طبيبك أو ممرضتك أو الصيدلي للحصول على المشورة إذا لم تكن متأكدًا. ستعتمد الجرعة الموصوفة لك على العلاج الذي تتلقاه.
الجرعة الموصي بها هي:
العلاج والوقاية من الغثيان والقيء المرتبط بالعلاج الكيميائي أو العلاج الإشعاعي لعلاج السرطان
الكبار
خذ 8 ملغ من أوندانسيترون قبل ساعة أو ساعتين من العلاج ، متبوعًا بـ 8 ملغ من أوندانسيترون بعد 12 ساعة. يمكن تناول جرعة 8 مجم من أوندانسيترون مرتين يوميًا لمدة تصل إلى 5 أيام بعد العلاج. قد يقرر طبيبك أن يعطيك الجرعة الأولى كحقنة مباشرة قبل العلاج.
استخدم في الأطفال (6 أشهر من العمر وما فوق) والمراهقين
الجرعة فردية وتعتمد على وزن الطفل وحجمه وسطح جسمه ، ولكن يجب ألا تتجاوز الجرعة اليومية الإجمالية 32 مجم. سيقرر طبيبك الجرعة لطفلك. لمزيد من المعلومات انظر الملصق: الجرعة الموصى بها للطفل هي 8 مجم مرتين في اليوم حسب وزن الجسم ويمكن أن تعطى لمدة تصل إلى 5 أيام.
المواطنين من كبار السن
أوندانسيترون جيد التحمل لدى المرضى فوق سن 65 الذين يتلقون العلاج الكيميائي ، ولا حاجة لتعديل الجرعة.
الوقاية والعلاج من الغثيان والقيء التالي للعمليات الجراحية
الكبار
الجرعة المعتادة هي 16 مجم أوندانسيترون قبل العملية بساعة واحدة أو 8 مجم أوندانسيترون قبل العملية بساعة واحدة ، تليها جرعتان من 8 مجم كل 8 ساعات.
استخدم في الأطفال (من عمر شهر واحد وما فوق) والمراهقين
يوصى بإعطاء أوندانسيترون كحقنة ، وتعتبر الأشكال الصيدلانية الأخرى لهذا الدواء أكثر ملاءمة للأطفال ؛ إسأل طبيبك أو الصيدلي.
المواطنين من كبار السن
هناك خبرة محدودة في استخدام أوندانسيترون عند كبار السن ، ومع ذلك فإن أوندانسيترون جيد التحمل في المرضى الذين تزيد أعمارهم عن 65 عامًا والذين يتلقون العلاج الكيميائي (انظر القسم أعلاه).
المرضى الذين يعانون من أمراض الكلى أو انخفاض التمثيل الغذائي للسبارتين / debrisoquine
لا يلزم تعديل الجرعة في المرضى الذين يعانون من أمراض الكلى أو للمرضى غير القادرين على التمثيل الغذائي للسبارتين / debrisoquine.
مرضى الكبد
يجب ألا تتجاوز الجرعة اليومية الإجمالية 8 ملغ في اليوم إذا كنت تعاني من مشاكل متوسطة إلى شديدة في الكبد.
إذا استمر الشعور بالغثيان ، اتصل بطبيبك أو الصيدلي أو الممرضة.
طريقة التناول:
- ابتلاع الأقراص مع كوب من الماء
- Ondasetron متاح أيضًا للحقن.
إذا نسيت أن تأخذ Ondansetron Mylan Generics
- إذا نسيت تناول جرعة ، وشعرت بالغثيان أو القيء ، فتناولها حالما تتذكرها. بعد ذلك ، خذ جهازك اللوحي التالي في الوقت المعتاد (كما هو موضح على الملصق). ومع ذلك ، إذا كان وقت الجرعة التالية قد حان بالفعل ، فتجاوز الجرعة الفائتة واستمر كالمعتاد.
لا تأخذ جرعة مضاعفة لتعويض الجرعة المنسية.
- إذا نسيت جرعة ولكن لا تشعر بالغثيان ، تناول الجرعة التالية كما هو موضح في الملصق.
لا تأخذ جرعة مضاعفة لتعويض الجرعة المنسية.
إذا توقفت عن تناول Ondansetron Mylan Generics
يجب ألا تتوقف عن تناول هذا الدواء ما لم يخبرك طبيبك بذلك. قد تتكرر الأعراض.
الجرعة الزائدة ماذا تفعل إذا تناولت الكثير من عقار أوندانسيترون - أدوية عامة
إذا تناولت أنت أو طفلك المزيد من Ondansetron Mylan Generics أكثر مما ينبغي
اتصل بطبيبك أو أقرب قسم طوارئ على الفور. خذ معك علبة الدواء وأي أقراص متبقية معك. هناك معلومات محدودة عن جرعة زائدة من أوندانسيترون. تشمل علامات الجرعة الزائدة التي تم الإبلاغ عنها مشاكل بصرية ، إمساك حاد ، انخفاض ضغط الدم الذي يمكن أن يسبب الدوار أو الإغماء وعدم انتظام ضربات القلب.
الآثار الجانبية ما هي الآثار الجانبية لل Ondansetron - الأدوية الجنيسة
مثل جميع الأدوية ، يمكن أن يسبب هذا الدواء آثارًا جانبية ، على الرغم من عدم حدوثها لدى الجميع.
قد تحدث الأعراض الجانبية الخطيرة التالية أثناء تناول هذا الدواء ، إذا لاحظت أيًا من هذه الآثار الجانبية ، فتوقف عن تناول الدواء واستشر الطبيب فورًا أو اذهب إلى أقرب مستشفى.
نادرة (قد تظهر لدى حتى 1 من كل 1000 شخص)
- إذا كان لديك رد فعل تحسسي ، فإن العلامات تشمل:
- صفير مفاجئ وألم في الصدر أو ضيق في الصدر
- انتفاخ الجفون أو الوجه أو الشفتين أو الفم أو اللسان
- متسرع
- بقع حمراء أو كتل تحت الجلد (خلايا النحل) في أي مكان من الجسم
- انهيار
غير شائعة (قد تظهر لدى حتى 1 من كل 100 شخص)
- حركات العين اللاإرادية (أزمة العين)
الآثار الجانبية المحتملة الأخرى
شائعة جدًا (قد تظهر لدى أكثر من 1 من كل 10 أشخاص):
- صداع الراس.
شائعة (قد تظهر لدى حتى 1 من كل 10 أشخاص):
- إمساك
- الشعور بالدفء أو الاحمرار
غير شائعة (قد تظهر لدى حتى 1 من كل 100 شخص):
- تنهدات
- انخفاض ضغط الدم ، مما قد يجعلك تشعر بالإغماء أو بالدوار
- عدم انتظام ضربات القلب أو بطء ضربات القلب
- ألم في الصدر مع أو بدون تغييرات في مخطط كهربية القلب
- النوبات ، حركات الجسم غير العادية أو الرعاش
- تشنجات العضلات
- تغييرات في اختبارات الدم تظهر تغيرات في طريقة عمل الكبد (في كثير من الأحيان في المرضى الذين يتلقون العلاج الكيميائي سيسبلاتين)
نادرة (قد تظهر لدى حتى 1 من كل 1000 شخص):
- رؤية ضبابية مؤقتة
- مشاكل في ضربات القلب تسمى إطالة فترة QT (تأخر توصيل الإشارات الكهربائية ، والتي يمكن رؤيتها على مخطط كهربية القلب ، تسجيل كهربائي للقلب). في بعض الأشخاص يمكن أن يؤدي هذا إلى مرض قلبي خطير يُعرف باسم torsades de pointes. وهذا يمكن يؤدي إلى ضربات قلب سريعة جدًا مما يؤدي إلى فقدان الوعي.
نادرة جدًا (قد تظهر لدى حتى 1 من بين 10000 شخص):
- ضعف الرؤية أو فقدان مؤقت للرؤية والذي عادة ما يتم حله في غضون 20 دقيقة
- ضربات قلب سريعة غير طبيعية
التأثيرات غير المرغوب فيها عند الأطفال والمراهقين
كانت الآثار الجانبية المبلغ عنها لدى الأطفال والمراهقين مشابهة جدًا لتلك التي لوحظت عند البالغين وتم الإبلاغ عنها في القائمة أعلاه.
التبليغ عن الأعراض الجانبية
إذا ظهرت عليك أي آثار جانبية ، تحدث إلى طبيبك أو الصيدلي أو الممرضة ، وهذا يشمل أي آثار جانبية محتملة غير مدرجة في هذه النشرة.يمكنك أيضًا الإبلاغ عن الآثار الجانبية مباشرة من خلال نظام الإبلاغ الوطني على www.agenziafarmaco.gov. / مسؤول. من خلال الإبلاغ عن الآثار الجانبية ، يمكنك المساعدة في توفير مزيد من المعلومات حول سلامة هذا الدواء.
انتهاء الصلاحية والاحتفاظ
احفظ هذا الدواء بعيدًا عن رؤية ومتناول أيدي الأطفال.
لا يتطلب هذا الدواء أي شروط تخزين خاصة. لا تستخدم هذا الدواء بعد تاريخ انتهاء الصلاحية المذكور على العبوة والعلبة بعد كلمة "EXP". يشير تاريخ انتهاء الصلاحية إلى اليوم الأخير من نفس الشهر.
لا تقم بإلقاء أي أدوية في مياه الصرف الصحي أو النفايات المنزلية ، اسأل الصيدلي عن كيفية التخلص من الأدوية التي لم تعد تستخدمها ، فهذا سيساعد في حماية البيئة.
الموعد النهائي "> معلومات أخرى
ما يحتويه Ondansetron Mylan Generics
- العنصر النشط هو أوندانسيترون.
يحتوي كل قرص على التوالي على 4 ملغ أو 8 ملغ من المادة الفعالة أوندانسيترون (على شكل هيدروكلوريد ثنائي هيدرات)
- المكونات الأخرى هي: اللاكتوز أحادي الهيدرات (انظر القسم 2 "Ondansetron Mylan Generics يحتوي على اللاكتوز مونوهيدرات") ، السليلوز الجريزوفولفين ، نشا الذرة المرن مسبقًا ، وستيرات المغنيسيوم.
يحتوي الطلاء على هيدروكسي بروبيل ، وثاني أكسيد التيتانيوم (E 171) ، وهيدروكسي بروبيل السليلوز ، وماكروغول ، وسوربيتان أوليات ، وحمض السوربيك ، والفانيلين ، والكينولين الأصفر (E 104).
كيف يبدو Ondansetron Mylan Generics وما هي محتويات العبوة
قرص 4 ملغ: قرص مطلي بلون أصفر شاحب ، مستدير ومحدب من الجانبين ، منقوش عليه "41" على جانب واحد.
قرص 8 ملغ: قرص مطلي بلون أصفر باهت ، مستدير ومحدب من الجانبين ، منقوش عليه "42" على جانب واحد.
حزم نفطة:
4 ملغ: 3 ، 6 ، 9 ، 10 ، 14 ، 15 ، 20 ، 30 ، 40 ، 50 ، 60 ، 90 ، 100 ، 200 ، 300 ، 500 قرص مغلف.
8 ملغ: 3 ، 6 ، 9 ، 10 ، 14 ، 15 ، 20 ، 30 ، 40 ، 50 ، 60 ، 90 ، 100 ، 200 ، 300 ، 500 قرص مغلف.
قد لا يتم تسويق جميع أحجام العبوات.
نشرة حزمة المصدر: AIFA (وكالة الأدوية الإيطالية). تم نشر المحتوى في يناير 2016. المعلومات الموجودة قد لا تكون محدثة.
للوصول إلى أحدث إصدار ، يُنصح بالوصول إلى موقع AIFA (وكالة الأدوية الإيطالية). إخلاء المسؤولية والمعلومات المفيدة.
01.0 اسم المنتج الطبي -
أقراص ONDANSETRONE MYLAN GENERICS مغلفة بالفيلم
02.0 التركيب النوعي والكمي -
أقراص مغلفة بالفيلم Ondansetron Mylan Generics 4 ملغ.
يحتوي كل قرص مغلف بالفيلم على 4 ملغ من أوندانسيترون (على شكل ثنائي هيدرات أوندانسيترون هيدروكلوريد).
سواغ ذات تأثير معروف: يحتوي كل قرص على 84.50 ملغ لاكتوز مونوهيدرات.
أقراص مغلفة بالفيلم Ondansetron Mylan Generics 8 ملغ.
يحتوي كل قرص مغلف بالفيلم على 8 ملغ أوندانسيترون (على شكل ثنائي هيدرات أوندانسيترون هيدروكلوريد).
سواغ ذات تأثير معروف: يحتوى كل قرص على 169.00 مجم لاكتوز مونوهيدرات.
للحصول على قائمة كاملة من السواغات ، انظر القسم 6.1.
03.0 الشكل الصيدلاني -
مضغوطة ملبسة بالفيلم.
كل قرص مطلي بالفيلم 4 ملغ لونه أصفر باهت ، مستدير ، محدب من الجانبين ، منقوش بالرمز "41" على جانب واحد.
كل قرص 8 ملغ مغلف بالفيلم أصفر شاحب ، مستدير ، محدب من الجانبين ، منقوش عليه "42" على جانب واحد.
04.0 معلومات سريرية -
04.1 المؤشرات العلاجية -
الكبار
يوصف أوندانسيترون لعلاج الغثيان والقيء الناجم عن العلاج الكيميائي السام للخلايا والعلاج الإشعاعي وللوقاية والعلاج من الغثيان والقيء بعد الجراحة (PONV).
سكان الأطفال
يوصف أوندانسيترون لعلاج الغثيان والقيء الناجم عن العلاج الكيميائي (CINV) عند الأطفال بعمر 6 أشهر وللوقاية والعلاج من الغثيان والقيء بعد الجراحة (PONV) عند الأطفال الذين تتراوح أعمارهم بين شهر واحد.
04.2 الجرعة وطريقة الإدارة -
الجرعة
يسبب العلاج الكيميائي والعلاج الإشعاعي الغثيان والقيء.
الكبار
تختلف القدرة المقيئة لعلاج السرطان وفقًا للجرعات ومجموعات العلاج الكيميائي وأنظمة العلاج الإشعاعي المستخدمة. يجب أن يكون مسار الإعطاء والجرعة من أوندانسيترون مرنًا ويتم اختياره وفقًا لما يلي.
العلاج الكيميائي والعلاج الإشعاعي المقيئ
في المرضى الذين يتلقون العلاج الكيميائي أو العلاج الإشعاعي المقيئ ، يمكن إعطاء أوندانسيترون إما عن طريق الفم أو في الوريد.
بالنسبة لمعظم المرضى الذين يتلقون علاجًا كيميائيًا أو علاجًا إشعاعيًا مقيئًا ، يجب في البداية إعطاء أوندانسيترون عن طريق الوريد مباشرة قبل العلاج متبوعًا بـ 8 ملغ عن طريق الفم كل 12 ساعة.
للإعطاء عن طريق الفم: 8 مجم قبل العلاج بساعة إلى ساعتين ، تليها 8 مجم بعد 12 ساعة.
للحماية من التقيؤ المتأخر أو المطول بعد الـ 24 ساعة الأولى ، يجب أن يستمر العلاج عن طريق الفم مع أوندانسيترون لمدة تصل إلى 5 أيام بعد العلاج.
العلاج الكيميائي المقيئ للغاية
في المرضى الذين يتلقون علاجًا كيميائيًا عالي التولد ، على سبيل المثال. جرعات عالية من سيسبلاتين ، يمكن أن تدار أوندانسيترون عن طريق الوريد.
للحماية من التقيؤ المتأخر أو المطول بعد الـ 24 ساعة الأولى ، يجب أن يستمر العلاج عن طريق الفم مع أوندانسيترون لمدة تصل إلى 5 أيام بعد العلاج.
الجرعة الموصى بها للإعطاء عن طريق الفم هي 8 مجم مرتين يومياً.
سكان الأطفال
CINV في الأطفال الذين تتراوح أعمارهم بين 6 أشهر والمراهقين:
يمكن حساب جرعة CINV على أساس مساحة سطح الجسم (BSA) أو الوزن - انظر أدناه. ينتج عن الجرعات القائمة على الوزن إجمالي جرعات يومية أعلى من الجرعة المستندة إلى مساحة سطح الجسم (انظر القسمين 4.4 و 5.1).
يجب تخفيف Ondansetron Mylan Generics للتسريب في 5 ٪ سكر العنب أو 0.9 ٪ كلوريد الصوديوم أو سوائل التسريب المماثلة الأخرى ويتم تسريبها في الوريد لمدة لا تقل عن 15 دقيقة.
لا توجد بيانات من التجارب السريرية الخاضعة للرقابة حول استخدام Ondasetron Mylan Generics في الوقاية من الغثيان والقيء المتأخر أو لفترات طويلة الناجم عن العلاج الكيميائي.لا توجد بيانات من التجارب السريرية الخاضعة للرقابة حول استخدام Ondasetron Mylan Generics للغثيان والقيء. عن طريق العلاج الإشعاعي عند الأطفال.
الجرعة محسوبة من قبل BSA
يجب إعطاء Ondasetron Mylan Generics مباشرة قبل العلاج الكيميائي كجرعة وريدية واحدة تبلغ 5 مجم / متر مربع. يجب ألا تزيد الجرعة في الوريد عن 8 ملغ.
يمكن أن تبدأ الجرعة الفموية بعد 12 ساعة وتستمر لمدة تصل إلى 5 أيام (انظر الجدول 1 أدناه).
يجب ألا تتجاوز الجرعة اليومية الكلية جرعة البالغين 32 مجم.
الجدول 1: جرعة BSA المستندة إلى العلاج الكيميائي - الأطفال الذين تتراوح أعمارهم بين 6 أشهر والمراهقين
أ: يجب ألا تزيد الجرعة في الوريد عن 8 ملغ.
ب: يجب ألا تزيد الجرعة اليومية الكلية عن جرعة البالغين 32 مجم.
الجرعة محسوبة على وزن الجسم
تؤدي الجرعات المستندة إلى الوزن إلى جرعة يومية إجمالية أعلى من الجرعة المستندة إلى مساحة سطح الجسم - انظر القسمين 4.4 و 5.1.
يجب إعطاء Ondasetron Mylan Generics مباشرة قبل العلاج الكيميائي كجرعة وريدية واحدة تبلغ 0.15 مجم / كجم. يجب ألا تزيد الجرعة في الوريد عن 8 ملغ.
يمكن إعطاء جرعتين أخريين في الوريد خلال فترة 4 ساعات.
يجب ألا تتجاوز الجرعة اليومية الكلية جرعة البالغين 32 مجم.
يمكن أن تبدأ الجرعة الفموية بعد 12 ساعة وتستمر لمدة تصل إلى 5 أيام (انظر الجدول 2).
الجدول 2: الجرعة المعتمدة على الوزن للعلاج الكيميائي - الأطفال الذين تقل أعمارهم عن 6 أشهر والمراهقين
أ: يجب ألا تزيد الجرعة في الوريد عن 8 ملغ.
ب: يجب ألا تتجاوز الجرعة اليومية الكلية جرعة البالغين 32 مجم.
المواطنين من كبار السن
يعتبر أوندانسيترون جيد التحمل في المرضى الذين تزيد أعمارهم عن 65 عامًا ولا يلزم إجراء أي تغييرات في الجرعة أو التكرار أو طريقة الإعطاء.
انظر أيضًا "مجموعات خاصة".
الغثيان والقيء بعد الجراحة (PONV)
الكبار
الوقاية من PONV
للوقاية من PONV ، يمكن إعطاء أوندانسيترون عن طريق الفم أو عن طريق الحقن في الوريد.
الإدارة عن طريق الفم:
- 16 مجم قبل التخدير بساعة
- بدلا من ذلك 8 ملغ قبل التخدير بساعة واحدة ، تليها جرعتان إضافيتان 8 ملغ بفاصل 8 ساعات.
علاج PONV في المكان
يوصى بالإعطاء عن طريق الوريد لعلاج PONV الموجود.
سكان الأطفال
الغثيان والقيء بعد الجراحة عند الأطفال بعمر 1 شهر والمراهقين
تركيبات عن طريق الفم
لم يتم إجراء أي دراسات حول استخدام أوندانسيترون الذي يتم تناوله عن طريق الفم في الوقاية من الغثيان والقيء التالي للعملية أو علاجهما ؛ ينصح بالحقن الوريدي البطيء لهذا الغرض.
حقنة:
للوقاية من PONV في مرضى الأطفال الذين يخضعون لعملية جراحية تحت التخدير العام ، يمكن إعطاء جرعة واحدة من أوندانسيترون عن طريق الحقن الوريدي البطيء (لا يقل عن 30 ثانية) بجرعة 0.1 مجم / كجم بحد أقصى 4 مجم. قبل أو بعد التخدير.
لعلاج PONV بعد الجراحة في مرضى الأطفال الذين يخضعون لعملية جراحية تحت التخدير العام ، يمكن إعطاء جرعة واحدة من Ondansetron Mylan Generics عن طريق الحقن الوريدي البطيء (لا تقل عن 30 ثانية) بجرعة 0.1 مجم / كجم بحد أقصى 4 مجم.
لا توجد بيانات عن استخدام ondansetron Mylan Generics في علاج القيء بعد الجراحة لدى الأطفال دون سن الثانية.
المواطنين من كبار السن
إن خبرة استخدام أوندانسيترون في الوقاية والعلاج من الغثيان والقيء بعد الجراحة (PONV) لدى كبار السن محدودة ، ومع ذلك فإن أوندانسيترون جيد التحمل في المرضى فوق سن 65 الذين يتلقون العلاج الكيميائي.
انظر أيضًا "مجموعات خاصة".
مجموعات خاصة
مرضى القصور الكلوي
لا يلزم إجراء تغييرات يومية في الجرعة أو التكرار أو مسار الإعطاء.
مرضى القصور الكبدي
في المرضى الذين يعانون من اختلال كبدي معتدل أو شديد ، تقل تصفية أوندانسيترون بشكل كبير ويطول عمر نصف المصل بشكل ملحوظ. في مثل هؤلاء المرضى لا ينبغي تجاوز الجرعة الإجمالية البالغة 8 ملغ في اليوم ولذلك يوصى بالإعطاء عن طريق الحقن أو الفم.
المرضى الذين يعانون من ضعف التمثيل الغذائي للسبارتين / debrisoquine
لا يتغير عمر النصف للتخلص من أوندانسيترون في المرضى المصنفين على أنهم مستقلبات ضعيفة من سبارتين و ديبريسوكين. وبالتالي ، فإن الجرعات المتكررة في هؤلاء المرضى ستعطي مستويات التعرض للأدوية لا تختلف عن تلك الخاصة بعامة السكان. لا يلزم إجراء تغييرات في الجرعة اليومية أو تكرار الإعطاء.
طريقة الإعطاء
استخدام عن طريق الفم.
04.3 موانع -
فرط الحساسية للمادة الفعالة أو لأي من السواغات المدرجة في القسم 6.1.
فرط الحساسية لمضادات مستقبلات 5-HT3 الانتقائية الأخرى (مثل جرانيسترون ، دولاسيترون).
الاستخدام المتزامن للأبومورفين (انظر القسم 4.5).
04.4 تحذيرات خاصة واحتياطات مناسبة للاستخدام -
تم الإبلاغ عن تفاعلات فرط الحساسية في المرضى الذين أظهروا فرط الحساسية لمضادات مستقبلات 5HT3 الانتقائية الأخرى.
يجب معالجة الأحداث التنفسية بأعراض ويجب أن يولي الأطباء اهتمامًا خاصًا لها باعتبارها سلائف لتفاعلات فرط الحساسية.
إطالة كيو تي
يطيل أوندانسيترون فترة QT بطريقة تعتمد على الجرعة (انظر القسم 5.1). بالإضافة إلى ذلك ، كانت هناك تقارير ما بعد التسويق عن torsade de pointes في المرضى الذين يتلقون ondansetron. تجنب استخدام أوندانسيترون في المرضى الذين يعانون من متلازمة كيو تي الطويلة الخلقية. يجب إعطاء أوندانسيترون بحذر في المرضى الذين لديهم أو قد يصابون بإطالة فترة QTc ، بما في ذلك المرضى الذين يعانون من اضطرابات الإلكتروليت ، وفشل القلب الاحتقاني ، واضطراب نظم القلب البطيء ، والاضطرابات ، والإيقاع أو التوصيل ، أو في المرضى الذين عولجوا بمضادات عدم انتظام ضربات القلب ، وعوامل منع بيتا الأدرينالية أو الأدوية الأخرى التي تؤدي إلى إطالة فترة QT أو إلى تشوهات الكهارل. يجب أيضًا توخي الحذر عند إعطاء Ondansetron Mylan Generics لمرضى القلب الذين يخضعون للتخدير المتزامن.
يجب تصحيح نقص بوتاسيوم الدم ونقص مغنسيوم الدم قبل إعطاء أوندانسيترون.
كانت هناك تقارير ما بعد التسويق لمرضى مصابين بمتلازمة السيروتونين (بما في ذلك الحالة العقلية المتغيرة ، وعدم الاستقرار اللاإرادي والتشوهات العصبية العضلية) بعد الاستخدام المتزامن لأوندانسيترون وأدوية أخرى لتحفيز السيروتونين (بما في ذلك مثبطات امتصاص السيروتونين الانتقائية (SSRIs)) ومثبطات امتصاص النوربينفرين والسيروتونين ( SNRIs).) إذا كان العلاج المتزامن مع أوندانسيترون وأدوية أخرى لتحفيز السيروتونين له ما يبرره سريريًا ، فيوصى بمراقبة المريض بشكل مناسب.
نظرًا لأنه من المعروف أن أوندانسيترون يزيد من وقت العبور في الأمعاء الغليظة ، يجب مراقبة المرضى الذين يعانون من علامات انسداد معوي تحت الحاد بعد الإعطاء.
لا يوصف أوندانسيترون للوقاية والعلاج من الغثيان والقيء بعد الجراحة عند الأطفال بعد جراحة البطن.
في المرضى الذين يخضعون لجراحة الغدة اللوزية ، فإن الوقاية من الغثيان والقيء باستخدام أوندانسيترون قد تخفي النزيف الخفي ، لذلك يجب متابعة هؤلاء المرضى عن كثب بعد إعطاء أوندانسيترون.
يجب استخدام Ondansetron Mylan Generics بحذر عند مرضى القصور الكبدي.
يجب عدم استخدام أقراص Ondansetron Mylan Generics المغلفة بالفيلم في الأطفال الذين تقل مساحة سطح الجسم الإجمالية عن 0.6 متر مربع.
سكان الأطفال
يجب مراقبة مرضى الأطفال الذين يتلقون أوندانسيترون مع عوامل العلاج الكيميائي السامة للكبد عن كثب لضعف وظائف الكبد.
الغثيان والقيء الناجم عن العلاج الكيميائي (CINV)
إذا تم حساب الجرعة بالوزن (مجم / كجم) وإذا تم إعطاء 3 جرعات على فترات 4 ساعات ، فإن الجرعة اليومية الكلية ستكون أعلى مما لو أعطيت جرعة واحدة 5 مجم / م 2 متبوعة بجرعة فموية. لم يتم التحقق من الفعالية النسبية لهاتين النظامين المختلفين للجرعة من خلال الدراسات السريرية.
تشير دراسات التوافق المتبادل إلى "فعالية مماثلة لكلا النظامين (انظر القسم 5.1).
سواغ ذات تأثير معروف
يحتوي Ondansetron Mylan Generics على اللاكتوز مونوهيدرات. المرضى الذين يعانون من مشاكل وراثية نادرة من عدم تحمل الجالاكتوز ، قصور lapp-lactase أو سوء امتصاص الجلوكوز والجالاكتوز يجب ألا يأخذوا هذا الدواء.
04.5 التفاعلات مع المنتجات الطبية الأخرى وأشكال التفاعل الأخرى -
لا يوجد دليل على أن أوندانسيترون يحرض أو يثبط عملية التمثيل الغذائي للمنتجات الطبية الأخرى التي يتم تناولها بشكل مشترك.أظهرت دراسات محددة أنه لا توجد تفاعلات عند تناول أوندانسيترون مع الكحول ، تيمازيبام ، فوروسيميد ، الفنتانيل ، ترامادول ، المورفين. البروبوفول.
يتم استقلاب أوندانسيترون عن طريق عدة إنزيمات سيتوكروم P-450 الكبدية: CYP3A4 و CYP2D6 و CYP1A2. يتم تعويض النقص الوراثي لـ CYP2D6) عادةً عن طريق إنزيمات أخرى ويجب أن تؤدي إلى تغييرات قليلة أو معدومة في التصفية الكلية للأوندانسيترون والجرعات المطلوبة. .
قد يؤدي استخدام أوندانسيترون مع الأدوية التي تطيل فترة QT إلى إطالة فترة QT التكميلية.الاستخدام المتزامن لأوندانسيترون مع الأدوية السامة للقلب (مثل أنثراسيكلين مثل دوكسوروبيسين أو داونوروبيسين أو تراستوزوماب) ، مضادات حيوية (مثل الإريثروميسين أو الكيتوكونزول) مثل الأميودارون) وحاصرات بيتا (مثل أتينولول أو تيمولول) قد تزيد من خطر عدم انتظام ضربات القلب (انظر القسم 4.4).
كانت هناك تقارير ما بعد التسويق عن مرضى مصابين بمتلازمة السيروتونين (بما في ذلك الحالة العقلية المتغيرة ، وعدم الاستقرار اللاإرادي والتشوهات العصبية العضلية) بعد الاستخدام المتزامن للأوندانسيترون وأدوية أخرى لتحفيز السيروتونين (بما في ذلك مثبطات استرداد السيروتونين الانتقائية ومثبطات استرداد السيروتونين الانتقائية). (انظر الفقرة 4.4)
أبومورفين: بناءً على تقارير عن انخفاض ضغط الدم الشديد وفقدان الوعي عند تناول أوندانسيترون مع أبومورفين هيدروكلوريد ، فإن الاستخدام المتزامن مع أبومورفين هو بطلان.
الفينيتوين وكاربامازيبين وريفامبيسين: في المرضى الذين عولجوا بمحفزات CYP3A4 القوية (مثل الفينيتوين ، الكاربامازيبين والريفامبيسين) تزداد التصفية الفموية للأوندانسيترون وتنخفض تركيزات أوندانسيترون في الدم.
ترامادول: تشير البيانات من دراسات صغيرة إلى أن أوندانسيترون قد يقلل من التأثير المسكن للترامادول.
04.6 الحمل والرضاعة:
حمل
لم يتم إثبات سلامة استخدام ondasetron في النساء الحوامل.
لا يشير تقييم الدراسات التي أجريت على الحيوانات التجريبية إلى آثار ضارة مباشرة أو غير مباشرة فيما يتعلق بتطور الجنين والجنين والحمل والنمو قبل وبعد الولادة.الرجال ، لا ينصح باستخدام ondasetron أثناء الحمل.
وقت الأكل
أظهرت الدراسات أن أوندانسيترون يُفرز في حليب الحيوانات المرضعة (انظر القسم 5.3) ، لذلك يوصى بعدم إرضاع الأمهات اللاتي يعالجن بالأوندانسيترون.
04.7 التأثيرات على القدرة على القيادة واستخدام الآلات -
في الاختبار الحركي النفسي ، لا يؤثر عقار أوندانسيترون على الأداء ولا يسبب التخدير ، ولا يتوقع حدوث أي تأثير سلبي على هذه الأنشطة بناءً على علم الأدوية من أوندانسيترون.
04.8 الآثار غير المرغوب فيها -
التأثيرات غير المرغوب فيها مدرجة أدناه وفقًا لفئة أعضاء النظام وتكرارها.
يتم تعريف الترددات على النحو التالي:
شائع جدا: (≥1 / 10)
شائع: (≥1 / 100 ص
غير شائع: (≥1 / 1،000 y
نادر: (1/10000 سنة
نادر جدا: (
غير معروف: (لا يمكن تقدير التردد من البيانات المتاحة)
الأحداث الشائعة جدًا والشائعة وغير الشائعة هي الأحداث التي يتم تحديدها بشكل عام أثناء التجارب السريرية. يؤخذ معدل حدوث الدواء الوهمي في الاعتبار ، والأحداث النادرة والنادرة جدًا هي الأحداث التي يتم تحديدها بشكل عام من خلال التقارير التلقائية خلال مرحلة ما بعد التسويق.
يتم تقدير الترددات التالية بالجرعات القياسية الموصى بها لاستخدام أوندانسيترون وفقًا للإشارات والصياغة.
تمت ملاحظتها مع عدم وجود دليل قاطع على وجود عقابيل سريرية مستمرة
² تم حل معظم حالات العمى المبلغ عنها في غضون 20 دقيقة ، وتم علاج العديد من المرضى بعوامل العلاج الكيميائي ، والتي تشمل سيسبلاتين ، وقد تم الإبلاغ عن بعض حالات العمى العابر على أنها قشرية المنشأ.
³ لوحظت هذه الحالات بشكل شائع عند المرضى الذين يتلقون العلاج الكيميائي لسيسبلاتين.
سكان الأطفال
إن المظهر الجانبي للحدث الضار لدى الأطفال والمراهقين يمكن مقارنته بتلك التي تظهر عند البالغين.
الإبلاغ عن ردود الفعل السلبية المشتبه بها
يعد الإبلاغ عن ردود الفعل السلبية المشتبه بها التي تحدث بعد الحصول على ترخيص من المنتج الطبي أمرًا مهمًا لأنه يسمح بالمراقبة المستمرة لتوازن الفوائد / المخاطر للمنتج الطبي. يُطلب من المتخصصين في الرعاية الصحية الإبلاغ عن أي ردود فعل سلبية مشتبه بها عبر نظام الإبلاغ. العنوان www. agenziafarmaco.gov.it/it/responsabili.
04.9 جرعة زائدة -
العلامات والأعراض
هناك خبرة محدودة مع جرعة زائدة من أونداسيترون ، في معظم الحالات ، كانت الأعراض مشابهة لتلك التي تم الإبلاغ عنها بالفعل في المرضى الذين يتلقون الجرعة الموصى بها (انظر القسم 4.8).
تشمل المظاهر التي تم الإبلاغ عنها الاضطرابات البصرية ، والإمساك الشديد ، وانخفاض ضغط الدم ، والحلقات الوعائية المبهمة مع إحصار عابر من الدرجة الثانية AV.
يطيل أوندانسيترون فترة QT بطريقة تعتمد على الجرعة. يوصى بمراقبة مخطط كهربية القلب في حالة تناول جرعة زائدة
علاج او معاملة
لا يوجد ترياق محدد للأوندانسيترون ، لذلك يجب توفير علاج مناسب وداعم للأعراض في جميع حالات الجرعة الزائدة المشتبه بها.
لا ينصح باستخدام عرق الذهب لعلاج جرعة زائدة من أوندانسيترون ، حيث من المحتمل أن لا يستجيب المرضى بسبب التأثير المضاد للقىء لأونداسيترون نفسه.
05.0 الخصائص الصيدلانية -
05.1 "الخصائص الديناميكية الدوائية -
المجموعة العلاجية: مضادات القيء ومضادات الآفات ومضادات السيروتونين (5HT3).
كود ATC: A04AA01.
آلية العمل
أوندانسيترون مضاد لمستقبلات 5-HT3 قوي وانتقائي للغاية.
آلية عملها الدقيقة لمضادات القيء والغثيان غير معروفة.يمكن أن تتسبب عوامل العلاج الكيميائي والعلاج الإشعاعي في إطلاق مادة السيروتونين (5-HT) من الأمعاء الدقيقة والتي بدورها ، عن طريق تنشيط الوصلات المبهمة من هرمون السيروتونين من خلال مستقبلات 5-HT3 ، يمكن أن تؤدي إلى منعكس الكمامة. يمنع أوندانسيترون بدء هذا المنعكس. علاوة على ذلك ، فإن تنشيط المسارات الواردة المبهم يمكن أن يحدد ، على مستوى منطقة postrema الموجودة في أرضية البطين الرابع ، إطلاق السيروتونين وهذا يمكن أن يحفز القيء من خلال آلية مركزية. لذلك ، فإن فعالية أوندانسيترون في علاج الغثيان والقيء الناجم عن العلاج الكيميائي السام للخلايا والعلاج الإشعاعي ترجع على الأرجح إلى تأثيره العدائي على مستقبلات 5HT3 من الخلايا العصبية الموجودة في كل من الجهاز العصبي المركزي والمحيطي.
آلية العمل في السيطرة على الغثيان والقيء بعد الجراحة غير معروفة ولكنها قد تكون مشابهة لآلية التحكم في الغثيان والقيء الناجمين عن السمية الخلوية.
في دراسة دوائية نفسية أجريت على متطوعين ، لم يظهر عقار أوندانسيترون تأثيرات مهدئة.
لا يغير أوندانسيترون من تركيزات البرولاكتين في البلازما.
لا يزال دور أوندانسيترون في التقيؤ الناجم عن المواد الأفيونية غير واضح.
سكان الأطفال
الغثيان والقيء الناجم عن العلاج الكيميائي (CINV)
تم تقييم فعالية أوندانسيترون في السيطرة على القيء والغثيان الناجم عن العلاج الكيميائي للسرطان في تجربة سريرية عشوائية مزدوجة التعمية في 415 مريضًا تتراوح أعمارهم بين 1 و 18 عامًا (S3AB3006).
في يوم العلاج الكيميائي ، تلقى المرضى أوندانسيترون 5 مجم / متر مربع في الوريد. + أوندانسيترون 4 مجم فموياً بعد 8 أو 12 ساعة أو أوندانسيترون 0.45 مجم / كجم فى الوريد. + دواء وهمي عن طريق الفم بعد 8 أو 12 ساعة.
بعد العلاج الكيميائي ، تلقت المجموعتان 4 مجم شراب أوندانسيترون مرتين في اليوم لمدة 3 أيام. كانت السيطرة الكاملة على التقيؤ في أسوأ يوم من العلاج الكيميائي 49٪ (5 مجم / م 2 IV + ondansetron 4 مجم عن طريق الفم) و 41٪ (0.45 مجم / كجم في الوريد + الدواء الوهمي عن طريق الفم).
بعد العلاج الكيميائي ، تلقت المجموعتان 4 مجم شراب أوندانسيترون مرتين في اليوم لمدة 3 أيام.
أظهرت تجربة سريرية عشوائية مزدوجة التعمية خاضعة للتحكم بالغفل (S3AB4003) في 438 مريضًا تتراوح أعمارهم بين 1 و 17 عامًا سيطرة كاملة على التقيؤ في أسوأ يوم من العلاج الكيميائي في:
• 73٪ من المرضى عند إعطاء أوندانسيترون عن طريق الوريد بجرعة 5 ملغ / م 2 في الوريد. مع 2-4 ملغ من ديكساميثازون عن طريق الفم
• 71٪ من المرضى تناولوا أوندانسيترون على شكل شراب بجرعة 8 ملغ + 2-4 ملغ ديكساميثازون عن طريق الفم في أيام العلاج الكيميائي).
بعد العلاج الكيميائي ، تلقت المجموعتان 4 مجم شراب أوندانسيترون مرتين في اليوم لمدة يومين.
تمت دراسة فعالية أوندانسيترون في 75 طفلاً تتراوح أعمارهم بين 6 إلى 48 شهرًا في دراسة مفتوحة غير قابلة للمقارنة بذراع واحدة (S3A40320). تلقى جميع الأطفال 3 جرعات من 0.15 مجم / كجم في الوريد من أوندانسيترون. تم إعطاؤه 30 دقيقة قبل البدء من العلاج الكيميائي ومتابعته 4 و 8 ساعات بعد الجرعة الأولى.
تم تحقيق السيطرة الكاملة على التقيؤ في 56٪ من المرضى.
دراسة أخرى مفتوحة التسمية غير مقارنة بذراع واحدة (S3A239) حققت في فعالية جرعة 0.15 مجم / كجم من أوندانسيترون متبوعة بجرعتين فموية من 4 مجم أونداسيترون للأطفال الذين تتراوح أعمارهم بين
تم تحقيق السيطرة الكاملة على التقيؤ في 42٪ من المرضى.
الوقاية من الغثيان والقيء بعد الجراحة (PONV)
تم التحقيق في فعالية جرعة واحدة من أوندانسيترون في الوقاية من الغثيان والقيء بعد الجراحة في دراسة عشوائية مزدوجة التعمية خاضعة للتحكم الوهمي في 670 طفلاً تتراوح أعمارهم بين 1 و 24 شهرًا (عمر ما بعد المفهوم ≥ 44 أسبوعًا ، الوزن 3 تم التخطيط لإجراء جراحة انتقائية تحت تأثير التخدير العام وكان مستوى ASA ≤ III. تم إعطاء جرعة واحدة من ondansetron 0.1 مجم / كجم خلال 5 دقائق من التخدير.كانت النسبة المئوية للأشخاص الذين عانوا من نوبة قيء واحدة على الأقل خلال فترة التقييم لمدة 24 ساعة (ITT) أعلى بالنسبة للمرضى الذين يتلقون العلاج الوهمي مقارنة بأولئك الذين يتلقون أوندانسيترون (28٪ مقابل 11٪ ، p.
أجريت أربع دراسات مزدوجة التعمية خاضعة للتحكم الوهمي في 1469 مريضًا من الذكور والإناث (من 2 إلى 12 عامًا) يخضعون للتخدير العام. تم اختيار المرضى بشكل عشوائي لجرعات وريدية واحدة من أوندانسيترون (0.1 مجم / كجم لمرضى الأطفال الذين يزنون 40 كجم أو أقل من 4 مجم لمرضى الأطفال الذين يزيد وزنهم عن 40 كجم ، عدد المرضى = 735) أو الدواء الوهمي (عدد المرضى = 734) . تم إعطاء عقار الدراسة خلال 30 ثانية على الأقل ، مباشرة قبل أو بعد تحريض التخدير ، وكان Ondansetron أكثر فعالية من العلاج الوهمي في منع الغثيان والقيء. تم تلخيص نتائج هذه الدراسات في الجدول 3.
الجدول 3: الوقاية والعلاج من PONV في مرضى الأطفال - علاج استجابة 24 ساعة
CR = لا توجد نوبة قيء أو إنقاذ أو انسحاب
05.2 "خصائص حركية الدواء -
بعد تناوله عن طريق الفم ، يمتص أوندانسيترون بشكل سلبي وكامل عن طريق الجهاز الهضمي ويخضع لعملية التمثيل الغذائي التمريري الأول (التوافر البيولوجي 60٪ تقريبًا). يبلغ تركيز البلازما الذروة بعد جرعة 8 مجم ، حوالي 30 نانوغرام / مل ، ووصل إلى ما يقرب من 1.5 ساعة بعد الإعطاء بالنسبة للجرعات التي تزيد عن 8 ملغ ، تكون الزيادة في التعرض الجهازي لأوندانسيترون مع زيادة الجرعة أكبر من الزيادة النسبية ؛ قد تعكس بعض الانخفاض في التمثيل الغذائي التمريري الأول عند الجرعات الفموية الأعلى. لم تتغير بمضادات الحموضة: أظهرت الدراسات التي أجريت على متطوعين كبار السن الأصحاء زيادة طفيفة ، ولكنها غير مهمة سريريًا ، مرتبطة بالعمر في كل من التوافر الحيوي الفموي (65٪) ونصف العمر (5 ساعات) لأوندانسيترون. لوحظت الفروق بين الجنسين في عملية التمثيل الغذائي للأوندانسيترون: تتمتع النساء بمعدل ودرجة أعلى من الامتصاص بعد تناول جرعة فموية وانخفاض في التخليص الجهازي وحجم التوزيع (المعدل حسب الوزن).
يتشابه توافر أوندانسيترون بعد الجرعات الفموية والعضلية والوريدية ، مع نصف عمر نهائي يبلغ حوالي 3 ساعات وحجم توزيع ثابت يبلغ 140 لترًا تقريبًا. يتم الحصول على التعرض الجهازي المكافئ بعد إعطاء أوندانسيترون عضليًا وريديًا.
أوندانسيترون غير مرتبط بدرجة عالية بالبروتين (70-76٪) لم يتم إثبات وجود علاقة مباشرة بين تركيزات البلازما والتأثير المضاد للقىء ، يتم تطهير أوندانسيترون من الدوران الجهازي في الغالب من خلال التمثيل الغذائي الكبدي عن طريق مسارات استقلابية متعددة. أقل من 5٪ من الجرعة الممتصة تفرز في البول دون تغيير. عدم وجود إنزيم CYP2D6 ( تعدد الأشكال debrisoquine) ليس له أي تأثير على الحرائك الدوائية للأوندانسيترون الخصائص الحركية الدوائية للأوندانسيترون لا تتغير بعد الجرعات المتكررة.
مجموعات خاصة
الأطفال والمراهقون (من شهر إلى 17 عامًا)
في مرضى الأطفال الذين تتراوح أعمارهم من 1 إلى 4 أشهر (ن = 19) الذين اضطروا للخضوع لعملية جراحية ، كان الوزن الطبيعي ، أقل بنسبة 30 ٪ تقريبًا من المرضى الذين تتراوح أعمارهم بين 5 إلى 24 شهرًا (ن = 22) ولكن يمكن مقارنتها بالمرضى الذين تتراوح أعمارهم بين 3 و 12 شهرًا سنوات. تم الإبلاغ عن نصف عمر المرضى الذين تتراوح أعمارهم من 1 إلى 4 أشهر بمتوسط 6.7 ساعة مقارنة بـ 2.9 ساعة للمرضى الذين تتراوح أعمارهم بين 5 إلى 24 شهرًا ومن 3 إلى 12 عامًا.
يمكن تفسير الاختلافات في المعلمات الحركية الدوائية في مجموعة المرضى الذين تتراوح أعمارهم بين 1 إلى 4 أشهر جزئيًا من خلال النسبة المئوية الأعلى من الماء عند الرضع والأطفال وحجم توزيع أكبر للمنتجات الطبية القابلة للذوبان في الماء مثل "أوندانسيترون".
في مرضى الأطفال الذين تتراوح أعمارهم بين 3 إلى 12 عامًا والذين يخضعون لجراحة انتقائية تحت التخدير العام ، تم تقليل القيم المطلقة لكل من التخليص وحجم التوزيع مقارنة بالقيم عند المرضى البالغين.
زاد كلا البارامترات خطيًا مع زيادة الوزن وبحلول عمر 12 عامًا ، كانت القيم تقترب من قيم الشباب.
عندما تم تطبيع قيم التصفية وحجم التوزيع حسب وزن الجسم ، كانت قيم هذه المعلمات متشابهة عبر الفئات العمرية في السكان. يعوض استخدام الجرعات القائمة على الوزن الاختلافات المرتبطة بالعمر وهو فعال في تطبيع التعرض الجهازي لدى مرضى الأطفال.
تم إجراء تحليل الحرائك الدوائية للسكان على 428 شخصًا (مرضى السرطان ومرضى الجراحة والمرضى الأصحاء) الذين تتراوح أعمارهم بين شهر واحد و 44 عامًا بعد إعطاء أوندانسيترون في الوريد. وبناءً على هذا التحليل ، فإن التعرض المنهجي (AUC) بعد الجرعات الفموية أو الوريدية من عقار أوندانسيترون في الأطفال و كان المراهقون مشابهين للبالغين ، باستثناء الأطفال الذين تتراوح أعمارهم من 1 إلى 4 أشهر ، وكان الحجم مرتبطًا بالعمر وكان أقل عند البالغين منه عند الرضع والأطفال. كان التخليص مرتبطًا بالوزن ، ولكن ليس العمر ، باستثناء الرضع من عمر 1 إلى 4 أشهر.
من الصعب استنتاج ما إذا كان هناك "انخفاض إضافي في التخليص المرتبط بالعمر عند الرضع من 1 إلى 4 أشهر أو مجرد تقلبات متأصلة بسبب انخفاض عدد الموضوعات التي تمت دراستها في هذه الفئة العمرية. نظرًا لأن المرضى الذين تقل أعمارهم عن 6 أشهر من العمر" سيتلقى جرعة واحدة فقط من PONV وقد لا يكون التخليص المخفض ذو صلة سريريًا.
فشل كلوي
في المرضى الذين يعانون من قصور كلوي (تصفية الكرياتينين 15-60 مل / دقيقة) ، يتم تقليل كل من التخليص النظامي وحجم التوزيع بعد إعطاء أوندانسيترون IV ، مما يؤدي إلى زيادة طفيفة ، ولكنها غير مهمة سريريًا ، في نصف عمر الإطراح. أظهرت دراسة أجريت على المرضى الذين يعانون من قصور كلوي حاد يتطلب غسيل كلوي منتظم (تمت دراسته بين الغسيل الكلوي) أن الحرائك الدوائية للأوندانسيترون لم تتغير إلى حد كبير بعد الإعطاء في الوريد.
كبار السن أو الفشل الكلوي
تقتصر الدراسات المحددة على كبار السن أو المرضى الذين يعانون من القصور الكلوي على الحقن الوريدي والتعاطي عن طريق الفم. ومع ذلك ، من المتوقع أن يكون نصف عمر أوندانسيترون بعد الإعطاء عن طريق المستقيم في هؤلاء السكان مشابهًا لتلك التي شوهدت عند المتطوعين الأصحاء ، حيث أن معدل التخلص من أوندانسيترون بعد الإعطاء المستقيمي لا يتم تحديده بالتخليص الجهازي.
قصور كبدي
بعد الإعطاء الفموي أو الوريدي أو العضلي في المرضى الذين يعانون من قصور كبدي حاد ، تقل التصفية الجهادية بشكل ملحوظ ، مع إطالة عمر النصف للتخلص (15-32 ساعة) والتوافر الحيوي الفموي يقترب من 100٪ بسبب انخفاض التمثيل الغذائي. لم يتم تقييم الحرائك الدوائية لأونداسينترون بعد تناوله على شكل تحاميل لدى مرضى القصور الكبدي.
05.3 بيانات السلامة قبل السريرية -
كشفت البيانات غير السريرية عن عدم وجود مخاطر خاصة على البشر بناءً على الدراسات التقليدية لعلم الأدوية الآمن ، والسمية بالجرعات المتكررة ، والسمية الجينية ، وإمكانية التسبب في السرطان.
يتراكم أوندانسيترون ومستقلباته في لبن الجرذان ، وتبلغ نسبة اللبن / البلازما 5.2.
أظهرت دراسة أجريت على القنوات القلبية للأيونات البشرية المستنسخة أن أوندانسيترون لديه القدرة على التدخل في عودة الاستقطاب القلبي عن طريق منع قنوات البوتاسيوم HERG. الصلة السريرية لهذه النتيجة غير واضحة. متطوعين (انظر القسم 5.1)
06.0 معلومات صيدلانية -
06.1 سواغ -
جوهر الأجهزة اللوحية:
مونوهيدرات اللاكتوز ، السليلوز الجريزوفولفين ، نشا الذرة ، ستيرات المغنيسيوم.
طلاء الأقراص:
هيبروميلوز ، ثاني أكسيد التيتانيوم (E171) ، هيدروكسي بروبيل سلولوز ، ماكروغول ، سوربيتان أوليات ، حمض السوربيك ، فانيلين ، كينولين أصفر (E104).
06.2 عدم التوافق "-
غير ذات صلة.
06.3 فترة الصلاحية "-
3 سنوات.
06.4 احتياطات خاصة للتخزين -
لا يتطلب هذا المنتج الطبي أي احتياطات تخزين خاصة.
06.5 طبيعة العبوة الفورية ومحتويات العبوة -
نفطة (PVC / AL)
4 مجم: 3 ، 6 ، 10 ، 14 ، 15 ، 20 ، 30 ، 40 ، 50 ، 60 ، 90 ، 100 ، 200 ، 300 و 500 قرص مغلف.
8 ملغ: 3 ، 6 ، 9 ، 10 ، 14 ، 15 ، 20 ، 30 ، 40 ، 50 ، 60 ، 90 ، 100 ، 200 ، 300 و 500 قرص مغلف.
قد لا يتم تسويق جميع أحجام العبوات.
06.6 تعليمات الاستخدام والتعامل -
لا توجد تعليمات خاصة.
يجب التخلص من الأدوية غير المستخدمة والمخلفات الناتجة وفقًا للوائح المحلية.
07.0 حائز على "ترخيص التسويق" -
Mylan S.p.A. - فيا فيتور بيساني ، 20-20124 ميلانو ، إيطاليا
08.0 رقم ترخيص التسويق -
4 ملغ أقراص مغلفة بالفيلم 3 أقراص من PVC / AL blister - AIC n. 037548017
4 ملغ أقراص مغلفة بالفيلم 6 أقراص في نفطة PVC / AL-AIC n. 037548029
4 ملغ أقراص مغلفة بالفيلم 10 أقراص في نفطة PVC / AL-AIC n. 037548031
4 ملغ 14 مضغوطة ملبسة بالفيلم في نفطة PVC / AL-AIC n. 037548043
4 ملغ مضغوطة ملبسة بالفيلم 15 قرصا من PVC / AL blister - AIC n. 037548056
4 مجم أقراص مغلفة بالفيلم 20 قرصاً من PVC / AL blister - AIC n. 037548068
4 ملغ مضغوطة ملبسة بالفيلم 30 مضغوطة من PVC / AL blister - AIC n. 037548070
4 ملغ مضغوطة ملبسة بالفيلم 40 قرصا في نفطة PVC / AL-AIC n. 037548082
4 ملغ مضغوطة ملبسة بالفيلم 50 قرصا في نفطة PVC / AL-AIC n. 037548094
4 ملغ أقراص مغلفة بالفيلم 60 قرصاً في نفطة PVC / AL-AIC n. 037548106
4 ملغ أقراص مغلفة بالفيلم 90 قرصاً في نفطة PVC / AL-AIC n. 037548118
4 ملغ أقراص مغلفة بالفيلم 100 قرص في نفطة PVC / AL-AIC n. 037548120
4 ملغ أقراص مغلفة بالفيلم 200 قرص في نفطة PVC / AL-AIC n. 037548132
4 ملغ أقراص مغلفة بالفيلم 300 قرص في نفطة PVC / AL-AIC n. 037548144
4 ملغ أقراص مغلفة بغشاء 500 قرص في نفطة PVC / AL-AIC n. 037548157
8 ملغ أقراص مغلفة بغشاء 3 أقراص في نفطة PVC / AL-AIC n. 037548169
8 ملغ أقراص مغلفة بالفيلم 6 أقراص في نفطة PVC / AL-AIC n. 037548171
8 ملغ أقراص مغلفة بالفيلم 10 أقراص في نفطة PVC / AL-AIC n. 037548183
8 ملغ 14 مضغوطة ملبسة بالفيلم في نفطة PVC / AL-AIC n. 037548195
8 ملغ مضغوطة ملبسة بالفيلم 15 قرصا في نفطة PVC / AL-AIC n. 037548207
8 مجم أقراص مغلفة بالفيلم 20 قرصاً في نفطة PVC / AL-AIC n. 037548219
8 ملغ مضغوطة ملبسة بالفيلم 30 قرصا في نفطة PVC / AL-AIC n. 037548221
8 ملغ أقراص مغلفة بالفيلم 40 قرصا في نفطة PVC / AL-AIC n. 037548233
8 مجم أقراص مغلفة بالفيلم 50 قرص في نفطة PVC / AL-AIC n. 037548245
8 ملغ أقراص مغلفة بالفيلم 60 قرصا في نفطة PVC / AL-AIC n. 037548258
8 مجم أقراص مغلفة بالفيلم 90 قرصاً في نفطة PVC / AL-AIC n. 037548260
8 ملغ أقراص مغلفة بالفيلم 100 قرص في نفطة PVC / AL-AIC n. 037548272
8 ملغ أقراص مغلفة بالفيلم 200 قرص في نفطة PVC / AL-AIC n. 037548284
8 ملغ أقراص مغلفة بالفيلم 300 قرص في نفطة PVC / AL-AIC n. 037548296
8 ملغ أقراص مغلفة بغشاء 500 قرص من مادة PVC / AL blister - AIC n. 037548308
4 مجم أقراص مغلفة بغشاء 9 أقراص في نفطة PVC / AL-AIC n. 037548310
8 مجم أقراص مغلفة بغشاء 9 أقراص في نفطة PVC / AL-AIC n. 037548322
09.0 تاريخ أول تفويض أو تجديد التفويض -
تشرين الثاني (نوفمبر) 2008
أكتوبر 2012
10.0 تاريخ مراجعة النص -
أغسطس 2015