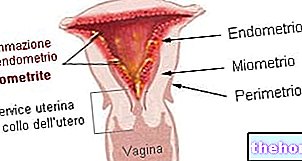
المكونات النشطة: إزيتيميب ، سيمفاستاتين
جولتور 10 مجم / 10 مجم
جولتور 10 مجم / 20 مجم
جولتور 10 مجم / 40 مجم
جلتور 10 ملجم / 80 ملجم
دواعي الإستعمال لماذا يتم استخدام Goltor؟ لما هذا؟
يحتوي جولتور على المواد الفعالة إيزيتميب وسيمفاستاتين. جولتور هو دواء يستخدم لخفض مستويات الكوليسترول الكلي والكوليسترول "الضار" (كوليسترول LDL) والمواد الدهنية التي تسمى الدهون الثلاثية في الدم. بالإضافة إلى ذلك ، يزيد الجولتور من مستويات الكوليسترول "الجيد" (كوليسترول البروتين الدهني عالي الكثافة).
يعمل GOLTOR بطريقتين لخفض الكوليسترول. المادة الفعالة ezetimibe تقلل من امتصاص الكوليسترول في الجهاز الهضمي. العنصر النشط سيمفاستاتين الذي ينتمي إلى فئة "الستاتين" يمنع إنتاج الكوليسترول الذي يصنعه الجسم.
الكوليسترول هو أحد المواد الدهنية العديدة الموجودة في مجرى الدم. يتكون الكوليسترول الكلي بشكل أساسي من كوليسترول البروتين الدهني منخفض الكثافة وكوليسترول البروتين الدهني عالي الكثافة. غالبًا ما يُطلق على كوليسترول البروتين الدهني منخفض الكثافة (LDL) اسم الكوليسترول "الضار" لأنه يمكن أن يتراكم في جدران الشرايين ويشكل لويحات. بمرور الوقت ، يمكن أن يؤدي تراكم هذه اللويحات إلى تضييق الشرايين. يمكن أن يؤدي هذا الضيق إلى إبطاء أو منع تدفق الدم إلى الأعضاء الحيوية مثل القلب والدماغ. يمكن أن يتسبب هذا الانسداد في تدفق الدم في حدوث نوبة قلبية أو سكتة دماغية.
غالبًا ما يطلق على كوليسترول البروتين الدهني عالي الكثافة (HDL) اسم الكوليسترول "الجيد" لأنه يساعد على منع تراكم الكوليسترول السيئ في الشرايين ويقي من أمراض القلب.
الدهون الثلاثية هي نوع آخر من الدهون في الدم يمكن أن تزيد من خطر الإصابة بأمراض القلب.
يستخدم GOLTOR للمرضى الذين لا يستطيعون التحكم في مستويات الكوليسترول لديهم من خلال النظام الغذائي وحده. أثناء تناول هذا الدواء ، لا يزال يتعين عليك اتباع نظام غذائي لخفض الكوليسترول.
يستخدم GOLTOR كإضافة لنظامك الغذائي لخفض الكوليسترول إذا كان لديك:
- ارتفاع مستويات الكوليسترول في الدم (فرط كوليسترول الدم الأولي) [متغاير الزيجوت العائلي وغير العائلي] أو ارتفاع مستويات الدهون في الدم (فرط شحميات الدم المختلط):
- الذين لا يخضعون لسيطرة جيدة من خلال الستاتين وحده ؛
- التي تناولت لها علاجًا بالستاتين وإيزيتيميب كأقراص منفصلة ؛
- مرض وراثي (فرط كوليسترول الدم العائلي متماثل الزيجوت) الذي يزيد من مستويات الكوليسترول في الدم. من الممكن أن تعالج بعلاجات أخرى أيضًا.
لا يساعدك جولتور على إنقاص الوزن.
موانع الاستعمال عندما لا ينبغي استخدام جولتور
لا تأخذ جولتور إذا:
- لديك حساسية (شديدة الحساسية) من "إيزيتيميب ، سيمفاستاتين أو أي من المكونات الأخرى لهذا الدواء
- يعاني حاليا من مشاكل في الكبد
- كنت حاملا أو مرضعة
- كنت تتناول دواء (أدوية) مع واحد أو أكثر من المواد الفعالة التالية:
- إيتراكونازول ، كيتوكونازول ، بوساكونازول أو فوريكونازول (يستخدم لعلاج الالتهابات الفطرية).
- الاريثروميسين ، كلاريثروميسين أو تيليثروميسين (يستخدم لعلاج الالتهابات).
- مثبطات الأنزيم البروتيني لفيروس نقص المناعة البشرية مثل إندينافير ونلفينافير وريتونافير وساكوينافير (تستخدم مثبطات إنزيم البروتياز لفيروس نقص المناعة البشرية لعلاج عدوى فيروس نقص المناعة البشرية)
- بوسيبريفير أو تيلابريفير (يستخدم لعلاج عدوى فيروس التهاب الكبد سي).
- نيفازودون (يستعمل لعلاج الإكتئاب).
- cobicistat
- جمفبروزيل (يستخدم لخفض الكوليسترول).
- السيكلوسبورين (غالبًا ما يستخدم في مرضى زراعة الأعضاء)
- دانازول (هرمون من صنع الإنسان يستخدم لعلاج الانتباذ البطاني الرحمي ، وهي حالة تنمو فيها بطانة الرحم خارج الرحم).
- كنت تتناول ، أو في الأيام السبعة الماضية ، تناولت أو تم إعطاؤك دواء يسمى حمض الفوسيديك (يستخدم لعلاج عدوى بكتيرية).
لا تأخذ أكثر من 10 ملغ / 40 ملغ من GOLTOR إذا كنت تتناول لوميتابيد (يستخدم لعلاج حالة الكوليسترول الوراثي الخطيرة والنادرة).
اطلب من طبيبك النصيحة إذا لم تكن متأكدًا مما إذا كان الدواء الذي تستخدمه هو أحد الأدوية المذكورة أعلاه.
احتياطات للاستخدام ما تحتاج إلى معرفته قبل تناول جولتور
أخبر طبيبك:
- لجميع حالاتك الطبية ، بما في ذلك الحساسية.
- إذا كنت تستهلك كميات كبيرة من الكحول أو إذا عانيت في الماضي من مرض كبدي. في هذه الحالة ، قد لا يكون GOLTOR مناسبًا لك.
- إذا كنت ستخضع لعملية جراحية. قد تحتاج إلى التوقف عن تناول GOLTOR لفترة قصيرة.
- إذا كنت آسيويًا ، فقد تكون جرعة مختلفة مناسبة لك.
يجب أن يقوم طبيبك بإجراء فحص دم قبل أن تأخذ GOLTOR وإذا كنت تعاني من أعراض مشاكل الكبد أثناء تناول GOLTOR. يتم إجراء هذا التحليل لمعرفة ما إذا كان الكبد يعمل بشكل صحيح.
قد يطلب طبيبك أيضًا إجراء اختبارات الدم للتحقق من وظائف الكبد بعد بدء العلاج بـ GOLTOR.
أثناء علاجك بهذا الدواء ، سيتحقق طبيبك بعناية من أنك لا تعاني من مرض السكري أو أنك لست عرضة للإصابة بمرض السكري. أنت معرض لخطر الإصابة بمرض السكري إذا كان لديك ارتفاع في مستويات السكر والدهون في الدم ، إذا كنت تعاني من زيادة الوزن وارتفاع ضغط الدم.
أخبر طبيبك إذا كان لديك مرض رئوي حاد. يجب تجنب استخدام GOLTOR مع الفايبريت (بعض أنواع الأدوية الخافضة للكوليسترول) حيث لم يتم دراسة استخدام GOLTOR مع الفايبريت.
اتصل بطبيبك على الفور إذا كنت تعاني من آلام في العضلات ، وحنان عضلي وضعف عضلي لأسباب غير محددة ، حيث يمكن أن تكون مشاكل العضلات ، في حالات نادرة ، شديدة وتؤدي إلى إصابة الأنسجة العضلية مما يؤدي إلى تلف الكلى ونادرًا ما تحدث الوفيات. يكون خطر إصابة العضلات أكبر عند الجرعات العالية من GOLTOR ، خاصة مع جرعة 10 مجم / 80 مجم.
كما أن خطر إصابة العضلات يكون أكبر لدى بعض المرضى. أخبر طبيبك إذا كان أي مما يلي ينطبق عليك:
- لديك مشاكل في الكلى
- لديك مشاكل في الغدة الدرقية
- يبلغ من العمر 65 عامًا أو أكبر
- أنثى
- عانيت من أي وقت مضى من مشاكل في العضلات أثناء العلاج بأدوية خفض الكوليسترول تسمى "الستاتين" (مثل سيمفاستاتين ، أتورفاستاتين ، وروزوفاستاتين) أو فيبرات (مثل جمفيبروزيل وبيزافيبرات)
- أنت أو عائلتك المقربين لديك مرض عضلي وراثي.
أخبر طبيبك أو الصيدلي أيضًا إذا كنت تعاني من ضعف مستمر في العضلات. قد تكون هناك حاجة إلى اختبارات وأدوية إضافية لتشخيص وعلاج هذه الحالة.
الأطفال والمراهقون
لا ينصح باستخدام GOLTOR للأطفال دون سن 10 سنوات.
التفاعلات أي الأدوية أو الأطعمة يمكن أن تعدل من تأثير جولتور
أخبر طبيبك إذا كنت تتناول أو تناولت مؤخرًا أو قد تتناول أي أدوية أخرى مع أي من المواد الفعالة التالية. قد يؤدي تناول GOLTOR مع أي من الأدوية التالية إلى زيادة خطر حدوث مشاكل في العضلات (تم ذكر بعضها أعلاه في قسم "لا تتناول GOLTOR إذا"):
- السيكلوسبورين (غالبًا ما يستخدم في المرضى الذين يخضعون لعملية زرع أعضاء)
- دانازول (هرمون من صنع الإنسان يستخدم لعلاج الانتباذ البطاني الرحمي ، وهي حالة تنمو فيها بطانة الرحم خارج الرحم)
- الأدوية التي تحتوي على مادة فعالة مثل إيتراكونازول ، كيتوكونازول ، فلوكونازول ، بوساكونازول أو فوريكونازول (تستخدم لعلاج الالتهابات الفطرية).
- الفايبريت مع المكونات النشطة مثل جمفيبروزيل وبيزافيبرات (تستخدم لخفض الكوليسترول)
- إريثروميسين ، كلاريثروميسين ، تيليثروميسين أو حمض الفوسيديك (يستخدم لعلاج الالتهابات البكتيرية). لا تأخذ حمض الفوسيديك أثناء استخدامك لهذا الدواء. انظر أيضا الفقرة 4 من هذه النشرة.
- مثبطات إنزيم البروتياز لفيروس نقص المناعة البشرية مثل إندينافير ونلفينافير وريتونافير وساكوينافير (المستخدمة لعلاج الإيدز)
- بوسيبريفير أو تيلابريفير (يستخدم لعلاج عدوى فيروس التهاب الكبد سي).
- نيفازودون (يستعمل لعلاج الإكتئاب).
- الأدوية التي تحتوي على المادة الفعالة كوبيسيستات
- الأميودارون (يستخدم لعلاج عدم انتظام ضربات القلب).
- فيراباميل ، ديلتيازيم أو أملوديبين (يستخدم لعلاج ارتفاع ضغط الدم وآلام الصدر المرتبطة بأمراض القلب أو أمراض القلب الأخرى).
- لوميتابيد (يستخدم لعلاج حالة كوليسترول وراثي خطيرة ونادرة
- جرعات عالية (1 جرام أو أكثر في اليوم) من النياسين أو حمض النيكوتين (يستخدم أيضًا لخفض الكوليسترول)
- كولشيسين (لعلاج النقرس).
بالإضافة إلى الأدوية المذكورة أعلاه ، يرجى إخبار طبيبك أو الصيدلي إذا كنت تتناول أو تناولت مؤخرًا أي أدوية أخرى ، بما في ذلك الأدوية التي تم الحصول عليها بدون وصفة طبية. على وجه الخصوص ، أخبر طبيبك إذا كنت تتناول أيًا مما يلي:
- الأدوية التي تحتوي على مادة فعالة لمنع تجلط الدم ، مثل وارفارين ، فلوينديون ، فينبروكومون أو أسينوكومارول (مضادات التخثر)
- كوليسترامين (يستخدم أيضًا لخفض الكوليسترول) لأنه يؤثر على طريقة عمل جولتور
- فينوفايبرات (يستخدم أيضًا لخفض الكوليسترول)
- ريفامبيسين (يستعمل لعالج السل).
يجب عليك أيضًا إخبار أي طبيب يصف دواءً جديدًا أنك تتناول GOLTOR.
مع الطعام والشراب
يحتوي عصير الجريب فروت على مادة أو أكثر تعمل على تغيير التمثيل الغذائي لبعض الأدوية ، بما في ذلك GOLTOR. يجب تجنب استهلاك عصير الجريب فروت لأنه يمكن أن يزيد من خطر حدوث مشاكل في العضلات.
تحذيرات من المهم معرفة ما يلي:
الحمل والرضاعة
لا تستخدمي GOLTOR إذا كنت حاملاً أو إذا كنت تنوي الحمل أو إذا كنت تشك في الحمل. إذا أصبحت حاملاً أثناء تناول GOLTOR ، فتوقف عن تناوله على الفور واتصل بطبيبك. لا ينبغي استخدام GOLTOR أثناء الرضاعة الطبيعية لأنه من غير المعروف ما إذا كان الدواء ينتقل إلى حليب الأم.
اسأل طبيبك أو الصيدلي للحصول على المشورة قبل تناول أي دواء.
السياقة واستعمال الماكنات
من غير المتوقع أن يتدخل GOLTOR في قدرتك على القيادة أو استخدام الآلات. ومع ذلك ، يجب أن يؤخذ في الاعتبار أن بعض الأشخاص قد عانوا من الدوار بعد تناول GOLTOR.
يحتوي جولتور على اللاكتوز
تحتوي أقراص GOLTOR على سكر ولاكتوز. إذا أخبرك طبيبك بأنك "لا تتحمل بعض السكريات ، فاتصل بطبيبك قبل تناول هذا الدواء.
الجرعة وطريقة الاستخدام كيفية استخدام جولتور: الجرعة
سيحدد طبيبك قوة الجهاز اللوحي المناسبة لك ، بناءً على علاجك الحالي وملف تعريف المخاطر الخاص بك.
الأقراص غير مكسورة ولا يجب تقسيمها.
احرص دائمًا على تناول هذا الدواء تمامًا كما أخبرك طبيبك أو الصيدلي. إذا كنت في شك ، استشر طبيبك أو الصيدلي.
- قبل البدء في تناول GOLTOR ، يجب أن تكون قد اتبعت بالفعل نظامًا غذائيًا لخفض مستويات الكوليسترول في الدم.
- أثناء العلاج بـ GOLTOR ، يجب أن تستمر في اتباع هذا النظام الغذائي لخفض نسبة الكوليسترول في الدم.
البالغون: الجرعة قرص واحد من جولتور عن طريق الفم مرة واحدة في اليوم.
الاستخدام لدى المراهقين (من 10 إلى 17 عامًا): الجرعة هي قرص واحد من GOLTOR عن طريق الفم مرة واحدة يوميًا (يجب عدم تجاوز الجرعة القصوى 10 مجم / 40 مجم مرة في اليوم).
يوصى بجرعة 10 مجم / 80 مجم من GOLTOR فقط للمرضى البالغين الذين يعانون من مستويات عالية جدًا من الكوليسترول والمعرضين لخطر الإصابة بأمراض القلب والذين لم يصلوا إلى مستوى الكوليسترول المثالي لديهم بأقل الجرعات.
خذ جولتور في المساء. يمكنك أن تأخذ مع أو بدون الطعام.
إذا وصف طبيبك GOLTOR مع دواء آخر لخفض الكوليسترول يحتوي على المادة الفعالة كوليستيرامين أو أي عامل عزل حمض الصفراء ، فيجب عليك تناول GOLTOR قبل ساعتين على الأقل أو بعد 4 ساعات من تناول عامل عزل حمض الصفراء.
إذا نسيت أن تأخذ GOLTOR
- لا تأخذ جرعة مضاعفة لتعويض قرص منسي ، فقط خذ جرعتك العادية من GOLTOR في اليوم التالي في الوقت المعتاد.
إذا توقفت عن تناول GOLTOR
- تحدث إلى طبيبك أو الصيدلي لأن نسبة الكوليسترول لديك قد ترتفع مرة أخرى. إذا كان لديك أي أسئلة أخرى حول استخدام هذا الدواء ، اسأل طبيبك أو الصيدلي.
الجرعة الزائدة ماذا تفعل إذا تناولت الكثير من جولتور
إذا تناولت كمية من الجولتور أكثر مما يجب عليك الاتصال بطبيبك أو الصيدلي.
الآثار الجانبية ما هي الآثار الجانبية لغولتور
مثل جميع الأدوية ، يمكن أن يتسبب GOLTOR في حدوث آثار جانبية ، على الرغم من عدم حدوثها لدى الجميع (انظر القسم 2 ما الذي تحتاج إلى معرفته قبل تناول GOLTOR).
تم الإبلاغ عن الآثار الجانبية الشائعة التالية (قد تؤثر على حتى 1 من كل 10 أشخاص):
- آلام العضلات
- زيادات في قيم الفحوصات المخبرية للدم لوظيفة الكبد (الترانساميناز) و / أو وظيفة العضلات (CK)
تم الإبلاغ عن الآثار الجانبية غير الشائعة التالية (قد تؤثر على ما يصل إلى 1 من كل 100 شخص):
- زيادة في قيم اختبارات الدم المتعلقة بوظائف الكبد ؛ زيادة في قيم حمض اليوريك في الدم ؛ زيادة في الوقت الذي يستغرقه الدم للتجلط ؛ وجود البروتين في البول ؛ انخفاض وزن الجسم
- دوخة صداع الراس؛ الاحساس بالوخز
- وجع بطن؛ عسر الهضم؛ انتفاخ؛ غثيان؛ انه يتقيأ انتفاخ البطن إسهال؛ فم جاف؛ ألم المعدة
- متسرع؛ حكة؛ الشرى
- الم المفاصل؛ ألم عضلي ؛ ضعف أو تشنجات الم الرقبة؛ ألم في الذراعين أو الساقين. آلام الظهر • التعب أو الضعف غير العادي. اشعر بالتعب؛ ألم صدر؛ انتفاخ ، وخاصة في اليدين والقدمين
- إختلال النوم؛ صعوبة في النوم
بالإضافة إلى ذلك ، تم الإبلاغ عن الآثار الجانبية التالية لدى الأشخاص الذين يتناولون GOLTOR أو الأدوية التي تحتوي على المواد الفعالة إيزيتيميب أو سيمفاستاتين:
- انخفاض عدد خلايا الدم الحمراء (فقر الدم). انخفاض عدد خلايا الدم ، والذي يمكن أن يسبب كدمات / نزيف (قلة الصفيحات)
- فقدان الإحساس أو الضعف في الذراعين والساقين ؛ ذاكره ضعيفه؛ فقدان الذاكرة؛ الالتباس
- مشاكل في التنفس بما في ذلك السعال المستمر و / أو ضيق التنفس أو الحمى
- إمساك
- التهاب البنكرياس في كثير من الأحيان مع آلام شديدة في البطن
- التهاب الكبد مع الأعراض التالية: اصفرار الجلد والعينين. حكة؛ بول داكن اللون أو براز فاتح اللون ؛ الشعور بالتعب أو الضعف فقدان الشهية؛ تليف كبدى؛ حصوات المرارة أو التهاب المرارة (الذي يمكن أن يسبب آلام في البطن والغثيان والقيء)
- تساقط شعر؛ طفح جلدي أحمر مرتفع ، أحيانًا مع آفات على شكل مستهدف (حمامي عديدة الأشكال)
- تفاعل فرط الحساسية الذي يشمل بعض الخصائص التالية: فرط الحساسية (تفاعلات حساسية تشمل تورم الوجه والشفتين واللسان و / أو الحلق الذي قد يسبب صعوبة في التنفس أو البلع ويتطلب علاجًا فوريًا ، ألم أو التهاب المفاصل ، التهاب الدم الأوعية الدموية ، كدمات غير طبيعية ، طفح جلدي وانتفاخ ، خلايا ، حساسية الجلد للشمس ، حمى ، احمرار ، ضيق في التنفس والشعور بالغثيان ، أعراض تشبه الذئبة (والتي تشمل طفح جلدي ، مشاكل جلدية) المفاصل ، وتأثيرات على خلايا الدم البيضاء).
- ألم عضلي؛ حساسية؛ ضعف العضلات أو تقلصات. إصابات العضلات مشاكل الأوتار ، وأحيانًا معقدة بسبب تمزق الأوتار.
- قلة الشهية
- الهبات الساخنة ضغط دم مرتفع
- وجع
- الضعف الجنسي لدى الرجال
- كآبة
- تغييرات في بعض قيم اختبارات الدم المتعلقة بوظائف الكبد
الآثار الجانبية المحتملة الإضافية المبلغ عنها مع بعض العقاقير المخفضة للكوليسترول:
- اضطرابات النوم ، بما في ذلك الكوابيس
- صعوبات جنسية
- داء السكري. من المرجح أن يكون لديك ارتفاع في مستويات السكر والدهون في الدم ، وزيادة الوزن وارتفاع ضغط الدم. سيراقبك طبيبك أثناء العلاج بهذا الدواء.
- ألم عضلي أو رقة أو ضعف مستمر قد لا يزول بعد إيقاف جولتور (التردد غير معروف).
اتصل بطبيبك على الفور إذا كنت تعاني من آلام في العضلات ، وحنان عضلي وضعف عضلي لأسباب غير محددة ، حيث يمكن أن تكون مشاكل العضلات ، في حالات نادرة ، شديدة وتؤدي إلى إصابة الأنسجة العضلية مما يؤدي إلى تلف الكلى ونادرًا ما تحدث الوفيات.
التبليغ عن الأعراض الجانبية
إذا ظهرت لديك أي أعراض جانبية ، تحدث إلى طبيبك أو الصيدلي ، وهذا يشمل أي آثار جانبية محتملة غير مذكورة في هذه النشرة. يمكنك أيضًا الإبلاغ عن الآثار الجانبية مباشرةً عبر نظام الإبلاغ الوطني على: www.agenziafarmaco.gov.it/it/responsabili من خلال الإبلاغ عن الآثار الجانبية ، يمكنك المساعدة في توفير مزيد من المعلومات حول سلامة هذا الدواء.
انتهاء الصلاحية والاحتفاظ
احفظ هذا الدواء بعيدًا عن رؤية ومتناول أيدي الأطفال.
لا تستخدم هذا الدواء بعد تاريخ انتهاء الصلاحية المدون على الحاوية بعد "EXP".
لا تقم بتخزين أقراص GOLTOR في درجات حرارة أعلى من 30 درجة مئوية.
البثور: يجب التخزين في العلبة الأصلية لحماية الدواء من الضوء والرطوبة.
الزجاجات: احفظ الزجاجات مغلقة بإحكام لحماية الدواء من الضوء والرطوبة.
لا تقم بإلقاء أي أدوية في مياه الصرف الصحي أو النفايات المنزلية ، اسأل الصيدلي عن كيفية التخلص من الأدوية التي لم تعد تستخدمها ، فهذا سيساعد في حماية البيئة.
معلومات أخرى
ماذا يفعل جولتور
المواد الفعالة لـ GOLTOR هي ezetimibe و simvastatin.
يحتوي كل قرص على 10 ملجم إيزيتيميب و 10 ملجم ، 20 ملجم ، 40 ملجم ، أو 80 ملجم سيمفاستاتين.
المكونات الأخرى هي: بوتيل هيدروكسي الأيسول ، أحادي الهيدرات حامض الستريك ، كروسكارميلوز الصوديوم ، هيدروكسي بروبيل ، اللاكتوز أحادي الهيدرات ، ستيرات المغنيسيوم ، السليلوز الجريزوفولفين ، بروبيل غالات.
وصف لشكل GOLTOR ومحتويات العبوة
يتوفر GOLTOR كأقراص بيضاء إلى بيضاء على شكل كبسولة مع الرمز "311" أو "312" أو "313" أو "315" على جانب واحد. الأقراص غير مكسورة ولا يجب تقسيمها.
يتوفر GOLTOR في عبوات من 7 ، 10 ، 14 ، 28 ، 30 ، 50 ، 56 ، 84 ، 90 ، 98 ، حزمة متعددة تحتوي على 98 (عبوتين من 49) ، 100 ، أو 300 قرص.
قد لا يتم تسويق جميع أحجام العبوات.
نشرة حزمة المصدر: AIFA (وكالة الأدوية الإيطالية). تم نشر المحتوى في يناير 2016. المعلومات الموجودة قد لا تكون محدثة.
للوصول إلى أحدث إصدار ، يُنصح بالوصول إلى موقع AIFA (وكالة الأدوية الإيطالية). إخلاء المسؤولية والمعلومات المفيدة.
01.0 اسم المنتج الطبي
أقراص جولتور
02.0 التركيب النوعي والكمي
يحتوي كل قرص على 10 ملغ من إيزيتيميب و 10 أو 20 أو 40 أو 80 ملغ من سيمفاستاتين.
سواغ:
كل قرص 10 ملغ / 10 ملغ يحتوي على 58.2 ملغ لاكتوز مونوهيدرات.
كل قرص 10 ملغ / 20 ملغ يحتوي على 126.5 ملغ لاكتوز مونوهيدرات.
كل قرص 10 ملغ / 40 ملغ يحتوي على 262.9 ملغ لاكتوز مونوهيدرات.
كل قرص 10 ملغ / 80 ملغ يحتوي على 535.8 ملغ لاكتوز مونوهيدرات.
للحصول على قائمة كاملة من السواغات ، انظر القسم 6.1.
03.0 الشكل الصيدلاني
لوح.
أقراص بيضاء إلى بيضاء ضاربة إلى الصفرة على شكل كبسولة مع الرمز "311" أو "312" أو "313" أو "315" على جانب واحد.
04.0 المعلومات السريرية
04.1 المؤشرات العلاجية
فرط كوليسترول الدم
يشار إلى GOLTOR كإضافة إلى النظام الغذائي في المرضى الذين يعانون من فرط كوليسترول الدم الأولي (العائلي وغير العائلي متغاير الزيجوت) أو مع فرط شحميات الدم المختلط حيث يشار إلى استخدام منتج مركب:
• المرضى الذين لا يخضعون للسيطرة الكافية على الستاتين وحده ؛
• المرضى الذين عولجوا بالفعل بعقار الستاتين وايزيتيميب.
يحتوي جولتور على إزيتيميب وسيمفاستاتين. ثبت أن Simvastatin (20-40 مجم) يقلل من تكرار الأحداث القلبية الوعائية (انظر القسم 5.1). لم يتم بعد إثبات التأثير المفيد لـ ezetimibe على المراضة القلبية الوعائية والوفيات.
فرط كوليسترول الدم العائلي متماثل الزيجوت (متماثل اللواقح)
يشار إلى GOLTOR كإضافة للنظام الغذائي في المرضى الذين يعانون من فرط كوليسترول الدم العائلي متماثل الزيجوت. قد يخضع المرضى أيضًا لتدابير علاجية إضافية (على سبيل المثال ، فصادة البروتين الدهني منخفض الكثافة [LDL]).
04.2 الجرعة وطريقة الإدارة
فرط كوليسترول الدم
يجب أن يتبع المريض نظامًا غذائيًا مناسبًا قليل الدسم ويجب أن يستمر في النظام الغذائي أثناء العلاج بـ GOLTOR.
يجب إعطاء الدواء عن طريق الفم. نطاق جرعة GOLTOR هو 10 ملغ / 10 ملغ / يوم إلى 10 ملغ / 80 ملغ / يوم في المساء.قد لا تتوفر جميع الجرعات في جميع الدول الأعضاء.الجرعة المعتادة هي 10 ملغ / 20 ملغ / يوم. o 10 ملغ / 40 ملغ / يوم تعطى في المساء كجرعة وحيدة.يوصى بجرعة 10 ملغ / 80 ملغ فقط في المرضى الذين يعانون من فرط كوليسترول الدم الحاد والمعرضين لخطر كبير من مضاعفات القلب والأوعية الدموية الذين لم يحققوا الأهداف العلاجية بجرعات أقل وعندما من المتوقع أن تفوق الفوائد المخاطر المحتملة (انظر الأقسام 4.4 و 5.1).
يجب مراعاة مستوى كوليسترول البروتين الدهني منخفض الكثافة (LDL-C) ، وخطر الإصابة بأمراض القلب التاجية ، واستجابة المريض للعلاج الحالي لخفض الكوليسترول في بداية العلاج أو عند تغيير الجرعة.
يجب أن تكون جرعة GOLTOR فردية بناءً على الفعالية المعترف بها للقوى المختلفة لـ GOLTOR (انظر القسم 5.1 ، الجدول 1) وعلى الاستجابة للعلاج المستمر لخفض الكوليسترول.يجب إجراء تعديلات الجرعة ، إذا لزم الأمر ، على فترات. أقل من 4 أسابيع يمكن تناول GOLTOR مع أو بدون وجبات.يجب عدم تقسيم الجهاز اللوحي.
فرط كوليسترول الدم العائلي متماثل الزيجوت
جرعة البدء الموصى بها للمرضى الذين يعانون من فرط كوليسترول الدم العائلي متماثل الزيجوت هي GOLTOR 10 مجم / 40 مجم / يوم في المساء. يوصى بجرعة 10 مجم / 80 مجم فقط عندما يُتوقع أن تفوق الفوائد المخاطر المحتملة (انظر أعلاه ؛ الأقسام 4.3 و 4.4). يمكن استخدام GOLTOR في هؤلاء المرضى كمساعد للعلاجات الأخرى الخافضة للدهون (على سبيل المثال ، فصادة LDL) أو إذا كانت هذه العلاجات غير متوفرة.
الإدارة المتزامنة مع المنتجات الطبية الأخرى
يجب أن يتم إعطاء GOLTOR إما قبل ساعتين أو بعد 4 ساعات من إعطاء عامل عزل حمض الصفراء.
في المرضى الذين يتناولون الأميودارون ، أملوديبين ، فيراباميل ، أو ديلتيازيم بالتزامن مع GOLTOR ، يجب ألا تتجاوز جرعة GOLTOR 10 مجم / 20 مجم / يوم (انظر القسمين 4.4 و 4.5).
في المرضى الذين يتلقون جرعات خافضة للدهون من النياسين (1 جم / يوم) بالتزامن مع GOLTOR ، يجب ألا تتجاوز جرعة GOLTOR 10 مجم / 20 مجم / يوم (انظر القسمين 4.4 و 4.5).
استخدم في كبار السن
لا يلزم تعديل الجرعة عند المرضى المسنين (انظر القسم 5.2).
استخدم في الأطفال والمراهقين
يجب أن يتم بدء العلاج تحت إشراف أخصائي.
المراهقون 10 سنوات (حالة البلوغ: الأولاد في المرحلة الثانية من تانر وما فوقها والفتيات اللائي تجاوزن فترة الحيض لمدة سنة واحدة على الأقل): الخبرة السريرية لدى مرضى الأطفال والمراهقين (10 إلى 17 عامًا) محدودة. ينصح بالبدء المعتاد. الجرعة 10 مجم / 10 مجم مرة واحدة يوميًا في المساء.نطاق الجرعة الموصى به هو 10 مجم / 10 مجم بحد أقصى 10 مجم / 40 مجم / يوم (انظر القسمين 4.4 و 5.2).
أطفال
استخدم في حالة تلف الكبد
لا يلزم تعديل الجرعة في حالات القصور الكبدي الخفيف (درجة Child-Pugh من 5 إلى 6). لا ينصح بالعلاج باستخدام GOLTOR في المرضى الذين يعانون من معتدلة (درجة Child-Pugh من 7 إلى 9) أو ضعف كبدي شديد. (درجة Child-Pugh> 9 ) ، (راجع الأقسام 4.4 و 5.2).
استخدم في حالة تلف الكلى
لا يلزم تعديل الجرعة في المرضى الذين يعانون من ضعف كلوي خفيف (معدل الترشيح الكبيبي المقدر ≥60 مل / دقيقة / 1.73 م 2). في المرضى الذين يعانون من أمراض الكلى المزمنة ومعدل الترشيح الكبيبي المقدر 2 ، فإن الجرعة الموصى بها من GOLTOR هي 10/20 مجم مرة واحدة يوميًا في المساء (انظر الأقسام 4.4 و 5.1 و 5.2). يجب إعطاء الجرعات العالية بحذر.
04.3 موانع الاستعمال
فرط الحساسية تجاه الإيزيتيميب أو سيمفاستاتين أو أي من السواغات.
الحمل والرضاعة (انظر القسم 4.6).
مرض الكبد النشط أو القيم المرتفعة والمستمرة وغير المحددة لترانس أميناس المصل.
الإعطاء المتزامن لمثبطات CYP3A4 القوية (العوامل التي تزيد من المساحة تحت المنحنى تقريبًا 5 أضعاف أو أكثر) (على سبيل المثال ، إيتراكونازول ، كيتوكونازول ، بوساكونازول ، فوريكونازول ، إريثروميسين ، كلاريثروميسين ، تيليثروميسين ، مثبطات إنزيم بروتياز فيروس نقص المناعة البشرية (مثل نلفينافير) ، بوسيبريفير) ، انظر القسمين 4.4 و 4.5).
الإدارة المصاحبة لـ gemfibrozil أو cyclosporine أو danazol (انظر القسمين 4.4 و 4.5).
04.4 تحذيرات خاصة واحتياطات مناسبة للاستخدام
اعتلال عضلي / انحلال الربيدات
تم الإبلاغ عن حالات اعتلال عضلي وانحلال الربيدات في تجربة ما بعد التسويق باستخدام ezetimibe. كان معظم المرضى الذين أصيبوا بانحلال الربيدات يخضعون للعلاج المتزامن مع ezetimibe والستاتين. ومع ذلك ، تم الإبلاغ عن انحلال الربيدات نادرًا جدًا باستخدام ezetimibe والعلاج الأحادي. ezetimibe للعوامل الأخرى المعروف أنها مرتبطة بزيادة خطر انحلال الربيدات.
يحتوي جولتور على سيمفاستاتين. سيمفاستاتين ، مثل مثبطات اختزال HMG-CoA الأخرى ، يسبب أحيانًا اعتلال عضلي ، يظهر على شكل ألم عضلي ، أو رقة ، أو ضعف مرتبط بارتفاع مستويات الكرياتين كيناز (CK) أعلى من 10 أضعاف الحد الأعلى الطبيعي. يظهر الاعتلال العضلي أحيانًا على شكل انحلال الربيدات مع أو بدون فشل كلوي حاد ثانوي لبيلة عضلية ونادراً ما تحدث نتائج مميتة. يزداد خطر الإصابة بالاعتلال العضلي بمستويات عالية من النشاط المثبط لانزيم HMG-CoA في البلازما.
كما هو الحال مع مثبطات اختزال HMG-CoA الأخرى ، فإن خطر الاعتلال العضلي / انحلال الربيدات هو جرعة مرتبطة بسيمفاستاتين. في قاعدة بيانات التجارب السريرية التي عولج فيها 41413 مريضًا بسيمفاستاتين ، تم تسجيل 24747 (حوالي 60٪) منهم في دراسات بمتوسط متابعة لمدة 4 سنوات على الأقل ، كان معدل الإصابة بالاعتلال العضلي حوالي 0.03٪ و 0.08٪ و 0.61٪ عند 20 و 40 و 80 ملغ / يوم على التوالي. في هذه الدراسات ، تمت مراقبة المرضى عن كثب واستبعدت بعض الأدوية المتفاعلة.
في دراسة سريرية تم فيها علاج المرضى الذين لديهم تاريخ من احتشاء عضلة القلب بسيمفاستاتين 80 ملغ / يوم (متوسط المتابعة 6.7 سنوات) ، كان معدل الإصابة بالاعتلال العضلي حوالي 1.0٪ مقارنة مع حدوث 0.02٪ في المرضى عولج بجرعة 20 ملغ / يوم ، ما يقرب من نصف حالات الاعتلال العضلي هذه حدثت خلال السنة الأولى من العلاج ، وبلغت نسبة حدوث الاعتلال العضلي خلال كل سنة تالية من العلاج حوالي 0.1٪ (انظر القسمين 4.8 و 5.1).
يكون خطر الإصابة بالاعتلال العضلي أعلى في المرضى الذين عولجوا بـ GOLTOR 10/80 mg مقارنة بالعلاجات الأخرى القائمة على الستاتين ذات الفعالية المماثلة في خفض LDL-C. لذلك ، يجب استخدام جرعة 10/80 مجم من GOLTOR فقط في المرضى الذين يعانون من فرط كوليسترول الدم الشديد والمعرضين لخطر الإصابة بمضاعفات القلب والأوعية الدموية الذين لم يحققوا أهداف العلاج بجرعات أقل وعندما يُتوقع أن تتجاوز الفوائد المخاطر المحتملة. في المرضى الذين عولجوا بـ GOLTOR 10/80 mg الذين يحتاجون إلى عامل تفاعلي ، يجب استخدام جرعة أقل من GOLTOR أو نظام الستاتين البديل مع احتمال أقل للتفاعلات الدوائية مع الأدوية (انظر أدناه. تدابير لتقليل خطر الإصابة بالاعتلال العضلي الناجم عن التفاعلات الدوائية والفقرات 4.2 و 4.3 و 4.5).
في دراسة سريرية تم فيها اختيار أكثر من 9000 مريض يعانون من أمراض الكلى المزمنة بصورة عشوائية لتلقي GOLTOR 10/20 ملغ يوميًا (العدد = 4650) أو الدواء الوهمي (العدد = 4620) (متوسط المتابعة 4.9 سنوات) ، l "حدوث اعتلال عضلي كان 0.2٪ لـ GOLTOR و 0.1٪ للعلاج الوهمي (انظر القسم 4.8).
في دراسة سريرية تم فيها علاج المرضى المعرضين لخطر الإصابة بأمراض القلب والأوعية الدموية بسيمفاستاتين 40 ملغ / يوم (متوسط المتابعة 3.9 سنوات) ، كان معدل الإصابة بالاعتلال العضلي حوالي 0.05٪ بالنسبة للمرضى غير الصينيين (العدد = 7،367) مقابل 0.24٪ للمرضى الصينيين (ن = 5468) بالرغم من أن السكان الآسيويين الوحيدين الذين تم تقييمهم في هذه الدراسة السريرية كانوا من الصينيين ، يجب توخي الحذر عند وصف GOLTOR للمرضى الآسيويين ويجب بالضرورة استخدام أقل جرعة.
انخفاض وظيفة نقل البروتينات
قد يؤدي انخفاض وظيفة بروتينات نقل OATP الكبدية إلى زيادة التعرض الجهازي لحمض سيمفاستاتين وزيادة خطر الإصابة بالاعتلال العضلي وانحلال الربيدات.قد يحدث خلل في الوظيفة نتيجة للتثبيط عن طريق الأدوية المتفاعلة (مثل السيكلوسبورين) وفي المرضى الذين يحملون النمط الجيني SLCO1B1 ج. 521 طنًا> ج.
المرضى الذين يحملون أليل الجين SLCO1B1 (c.521T> C) المشفرون لبروتين OATP1B1 الأقل نشاطًا زادوا من التعرض الجهازي لحمض سيمفاستاتين وخطر أكبر للإصابة بالاعتلال العضلي. يبلغ خطر الإصابة بالاعتلال العضلي المرتبط بجرعة عالية (80 مجم) من سيمفاستاتين حوالي 1٪ بشكل عام ، دون إجراء اختبار جيني. واستنادًا إلى نتائج دراسة البحث ، تم علاج ناقلات C متماثلة اللواقح (وتسمى أيضًا CC) بـ 80 مجم. 15٪ خطر الإصابة بالاعتلال العضلي في غضون عام واحد ، في حين أن الخطر في ناقلات الزيجوت غير المتجانسة للأليل C متغاير الزيجوت (CT) هو 1.5٪. الخطر النسبي هو 0.3٪ في المرضى الذين لديهم النمط الجيني الأكثر شيوعًا (TT) (انظر القسم 5.2). يجب مراعاة التنميط الجيني لوجود الأليل C كجزء من تقييم مخاطر الفوائد قبل وصف سيمفاستاتين 80 مجم للمرضى الأفراد والجرعات العالية ، عند أولئك الذين لديهم النمط الجيني CC ، عند توفرها. هذا الجين في التنميط الجيني لا يستبعد إمكانية تطور اعتلال عضلي.
قياس مستويات الكرياتين كيناز
لا ينبغي قياس مستويات CK بعد تمرين شاق أو في وجود أي سبب بديل لزيادة CK لأن هذا قد يجعل من الصعب تفسير البيانات. إذا كانت مستويات CK مرتفعة بشكل كبير عند خط الأساس (أكبر من 5 أضعاف الحد الأعلى الطبيعي) ، فيجب إعادة قياسها في غضون 5-7 أيام حتى يتم تأكيد النتائج.
قبل العلاج
يجب إبلاغ جميع المرضى الذين يبدأون علاج GOLTOR أو يزيدون جرعة GOLTOR بخطر الإصابة بالاعتلال العضلي وأن يُطلب منهم الإبلاغ عن أي ألم عضلي غير مبرر ، والحنان والضعف على الفور.
يجب توخي الحذر عند المرضى الذين لديهم عوامل مؤهبة لانحلال الربيدات. من أجل تحديد قيمة مرجعية أساسية ، يجب قياس مستوى CK قبل بدء العلاج في الحالات التالية:
• كبار السن (سن 65 سنة)
• الجنس الأنثوي
• تلف الكلى
• قصور الغدة الدرقية غير المنضبط
• التاريخ الشخصي أو العائلي لاضطرابات العضلات الوراثية
• تاريخ من نوبات سابقة من تسمم العضلات مع الستاتين أو الفايبريت
• مدمن كحول.
في الحالات المذكورة أعلاه ، يجب موازنة المخاطر التي ينطوي عليها العلاج مقابل الفائدة المحتملة ، ويوصى بمراقبة المريض عن كثب في حالة العلاج. إذا كان المريض قد عانى سابقًا من اضطرابات العضلات أثناء علاجه باستخدام مادة الفايبريت أو الستاتين ، فيجب أن يبدأ العلاج بأي منتج يحتوي على الستاتين (مثل GOLTOR) بحذر فقط. إذا كانت مستويات CK مرتفعة بشكل ملحوظ عند خط الأساس (أكبر من 5 أضعاف الحد الأعلى الطبيعي) ، فلا ينبغي بدء العلاج.
أثناء العلاج
إذا أبلغ المريض عن آلام في العضلات أو ضعف أو تقلصات أثناء العلاج بـ GOLTOR ، فيجب قياس مستويات CK. في حالة ارتفاع مستويات CK بشكل ملحوظ (أكبر من 5 أضعاف الحد الأعلى الطبيعي) ، في حالة عدم ممارسة التمارين الرياضية الشاقة ، يجب التوقف عن العلاج. يمكن النظر في وقف العلاج في حالة ظهور أعراض عضلية شديدة تسبب عدم الراحة اليومية ، حتى لو بقيت قيم CK أقل من 5 أضعاف الحد الأعلى الطبيعي.يجب التوقف عن العلاج إذا كان هناك اشتباه في اعتلال عضلي لأي سبب آخر.
إذا هدأت الأعراض وعادت مستويات CK إلى وضعها الطبيعي ، فيمكن النظر في إعادة إدخال GOLTOR ، أو منتج آخر يحتوي على ستاتين آخر ، بأقل جرعة وتحت المراقبة الدقيقة.
لوحظ ارتفاع معدل الإصابة بالاعتلال العضلي في المرضى الذين تمت معايرتهم إلى سيمفاستاتين 80 مجم (انظر القسم 5.1) ، ويوصى بقياس مستويات CK بشكل دوري لأنها قد تكون مفيدة في تحديد الحالات تحت السريرية للاعتلال العضلي. مثل هذه المراقبة سوف تمنع الاعتلال العضلي.
يجب إيقاف علاج GOLTOR مؤقتًا قبل أيام قليلة من الجراحة الاختيارية الكبرى وفي حالة ظهور أي حالة طبية أو جراحية كبيرة.
تدابير لتقليل خطر الإصابة بالاعتلال العضلي الناجم عن التفاعلات الدوائية (انظر أيضًا القسم 4.5)
يزداد خطر الإصابة بالاعتلال العضلي وانحلال الربيدات بشكل كبير من خلال الاستخدام المتزامن لـ GOLTOR مع مثبطات CYP3A4 القوية (مثل إيتراكونازول ، كيتوكونازول ، بوساكونازول ، فوريكونازول ، إريثروميسين ، كلاريثروميسين ، تليثرومايسين ، مثبطات إنزيم بروتياز فيروس نقص المناعة البشرية ، نيلفيفيرون). ) ، كما هو الحال مع السيكلوسبورين والدانازول والجيمفبروزيل. يمنع استخدام هذه الأدوية (انظر القسم 4.3).
نظرًا لوجود سيمفاستاتين في GOLTOR ، يزداد خطر الإصابة بالاعتلال العضلي وانحلال الربيدات أيضًا من خلال الاستخدام المتزامن لفيبرات أخرى ، النياسين بجرعات مخفضة للدهون (≥ 1 جم / يوم) أو عن طريق الاستخدام المتزامن للأميودارون ، أملوديبين ، فيراباميل أو ديلتيازيم مع بعض جرعات الجولتور (انظر القسمين 4.2 و 4.5). قد يزداد خطر الإصابة بالاعتلال العضلي ، بما في ذلك انحلال الربيدات عند تناول GOLTOR مع حمض الفوسيديك (انظر القسم 4.5).
وبالتالي ، فيما يتعلق بمثبطات CYP3A4 ، فإن الاستخدام المتزامن لـ GOLTOR مع إيتراكونازول ، كيتوكونازول ، بوساكونازول ، فوريكونازول ، مثبطات إنزيم بروتياز HIV (مثل nelfinavir) ، boceprevir ، telaprevir ، erythromycin ، عكس المقاطع 4.3 (انظر كلارفيثروميسين). إذا كان لا يمكن تجنب العلاج بمثبطات CYP3A4 القوية (العوامل التي تزيد من AUC حوالي 5 أضعاف أو أكثر) ، يجب التوقف عن العلاج بـ GOLTOR (وينبغي النظر في استخدام ستاتين آخر) أثناء بالإضافة إلى ذلك ، يجب توخي الحذر عند الجمع بين GOLTOR بعض مثبطات CYP3A4 الأخرى الأقل فاعلية: فلوكونازول ، فيراباميل ، ديلتيازيم (انظر القسمين 4.2 و 4.5) يجب تجنب تناول عصير الجريب فروت مع الجولتور.
لا ينبغي أن تدار سيمفاستاتين مع حمض الفوسيديك. كانت هناك تقارير عن انحلال الربيدات (بما في ذلك بعض الوفيات) في المرضى الذين يتلقون هذه المجموعة (انظر القسم 4.5). في المرضى الذين يعتبر استخدام حمض الفوسيديك الجهازي ضروريا ، يجب التوقف عن العلاج بالستاتين طوال فترة العلاج بحمض الفوسيديك ، وينبغي نصح المرضى بالحصول على رعاية طبية فورية في حالة ظهور أعراض ضعف العضلات أو الألم أو الرقة.
يمكن إعادة تقديم العلاج بالستاتين بعد سبعة أيام من الجرعة الأخيرة من حمض الفوسيديك. في الظروف الاستثنائية التي تتطلب الاستخدام الجهازي المطول لحمض الفوسيديك ، على سبيل المثال لعلاج الالتهابات الشديدة ، يجب تقييم الحاجة إلى التناول المشترك لـ GOLTOR وحمض الفوسيديك فقط على أساس كل حالة على حدة تحت إشراف طبي صارم.
يجب تجنب الاستخدام المتزامن لـ GOLTOR بجرعات أعلى من 10 مجم / 20 مجم في اليوم والنياسين بجرعات مخفضة للدهون (1 جم / يوم) ما لم يكن من المرجح أن تفوق الفائدة السريرية زيادة خطر الإصابة بالاعتلال العضلي (انظر القسمين 4.2 و 4.5 ).
ارتبطت حالات نادرة من اعتلال عضلي / انحلال الربيدات بالإعطاء المتزامن لمثبطات اختزال HMG-CoA والجرعات المعدلة للدهون من النياسين (حمض النيكوتينيك) (1 جم / يوم) ، وكلاهما يمكن أن يسبب اعتلال عضلي عند إعطاؤهما بمفردهما.
في دراسة سريرية (متابعة متوسطة تبلغ 3.9 سنوات) شملت مرضى معرضين لخطر الإصابة بأمراض القلب والأوعية الدموية ومستويات LDL-C مضبوطة جيدًا على simvastatin 40 ملغ / يوم مع أو بدون ezetimibe 10 ملغ ، لم تكن هناك فائدة إضافية على نتائج القلب والأوعية الدموية مع إضافة جرعات معدلة للدهون من النياسين (حمض النيكوتينيك) (1 جرام / يوم). لذلك ، يفكر الأطباء في العلاج المركب مع سيمفاستاتين وجرعات النياسين المعدل للدهون (حمض النيكوتينيك) (1 جم / يوم) أو يجب أن تزن المنتجات المحتوية على النياسين بعناية الفوائد والمخاطر المحتملة ويجب أن تراقب المرضى عن كثب بحثًا عن أي علامات أو أعراض لألم العضلات أو الحساسية أو الضعف ، خاصة خلال الأشهر الأولى من العلاج وعند زيادة جرعات أحد الأدوية أو الأدوية الأخرى .
بالإضافة إلى ذلك ، في هذه الدراسة ، كان معدل الإصابة بالاعتلال العضلي حوالي 0.24٪ للمرضى الصينيين الذين عولجوا بسيمفاستاتين 40 مجم أو إيزيتيميب / سيمفاستاتين 10/40 مجم مقارنة بـ 1.24٪ للمرضى الصينيين الذين عولجوا بسيمفاستاتين .40 مجم أو إيزيتيميب / سيمفاستاتين 10 / 40 مجم تدار بشكل مشترك مع حمض النيكوتينيك / لاروبيبرانت 2000 مجم / 40 مجم معدل الإطلاق. على الرغم من أن السكان الآسيويين الوحيدون الذين تم تقييمهم في هذه الدراسة السريرية هم الصينيون ، نظرًا لأن معدل الإصابة بالاعتلال العضلي أعلى في المرضى الصينيين منه في المرضى غير الصينيين ، فإن تناول GOLTOR المصاحب بجرعات من النياسين (حمض النيكوتين) يمكن أن يعدل ملف الدهون ( ≥ 1 جم / يوم) لا ينصح به للمرضى الآسيويين.
يرتبط Acipimox بنيوياً بالنياسين. على الرغم من عدم دراسة الأسيبيموكس ، إلا أن مخاطر التأثيرات السامة المرتبطة بالعضلات قد تكون مماثلة لتلك الخاصة بالنياسين.
يجب تجنب الاستخدام المتزامن لـ GOLTOR بجرعات أعلى من 10 مجم / 20 مجم يوميًا والأميودارون أو أملوديبين أو فيراباميل أو ديلتيازيم (انظر القسمين 4.2 و 4.5).
المرضى الذين يتناولون منتجات طبية أخرى معروفة بتأثير مثبط معتدل على CYP3A4 بجرعات علاجية عند استخدامها بالتزامن مع GOLTOR ، خاصة مع الجرعات العالية من GOLTOR ، قد يكون لديهم خطر متزايد للإصابة بالاعتلال العضلي. إذا تم تناول GOLTOR مع مثبط CYP3A4 معتدل (عوامل تزيد من المساحة تحت المنحنى تقريبًا 2-5 أضعاف) ، فقد يلزم تعديل الجرعة. بالنسبة لبعض مثبطات CYP3A4 المعتدلة مثل الديلتيازيم ، يوصى بجرعة قصوى تبلغ 10/20 مجم من GOLTOR (انظر القسم 4.2).
لم يتم دراسة سلامة وفعالية GOLTOR المعطى بالفايبرات.هناك خطر متزايد للإصابة بالاعتلال العضلي عند الاستخدام المتزامن لـ simvastatin و fibrates (خاصة gemfibrozil). لذلك ، فإن الاستخدام المتزامن لـ GOLTOR و gemfibrozil هو بطلان (انظر القسم 4.3) ولا ينصح بالاستخدام المتزامن مع الفايبريتات الأخرى (انظر القسم 4.5).
إنزيمات الكبد
في دراسات الجرعات المختلطة الخاضعة للرقابة والتي عولج فيها المرضى بإيزيتيميب وسيمفاستاتين ، لوحظت ارتفاعات متتالية في الترانساميناسات (3 أضعاف الحد الأعلى الطبيعي [ULN]) (انظر القسم 4.8).
في تجربة سريرية مضبوطة تم فيها اختيار أكثر من 9000 مريض يعانون من أمراض الكلى المزمنة عشوائياً لتلقي GOLTOR 10/20 ملغ يوميًا (ن = 4650) أو دواء وهمي (ن = 4620) (متوسط فترة المتابعة 4.9 سنوات) ، حدوث كانت ارتفاعات الترانساميناز المتتالية (> 3 مرات ULN) 0.7٪ لـ GOLTOR و 0.6٪ للعلاج الوهمي (انظر القسم 4.8).
يوصى بإجراء اختبارات وظائف الكبد قبل بدء العلاج بـ GOLTOR وبعد ذلك عند الإشارة سريريًا. يجب أن يخضع المرضى الذين تمت معايرتهم إلى جرعة 10 مجم / 80 مجم لاختبار إضافي قبل المعايرة ، وبعد 3 أشهر من المعايرة إلى جرعة 10 مجم / 80 مجم ، وبشكل دوري بعد ذلك (على سبيل المثال ، كل ستة أشهر) للسنة الأولى من العلاج. يجب إيلاء اهتمام خاص للمرضى الذين تظهر عليهم ارتفاعات في الترانساميناسات المصلية وفي هؤلاء المرضى يجب تكرار اختبارات الدم على الفور وإجراء المزيد من الاختبارات بعد ذلك. إذا أظهرت مستويات الترانس أميناز دليلاً على التقدم ، خاصةً إذا ارتفعت إلى 3 أضعاف ULN واستمرت ، فيجب إيقاف العلاج الدوائي. لاحظ أن ALT قد ينشأ من العضلات ، لذلك قد تشير الزيادة في ALT و CK إلى اعتلال عضلي (انظر أعلاه اعتلال عضلي / انحلال الربيدات).
كانت هناك تقارير نادرة بعد التسويق عن فشل كبدي مميت وغير مميت في المرضى الذين يتناولون العقاقير المخفضة للكوليسترول ، بما في ذلك سيمفاستاتين. إذا حدثت إصابة الكبد الشديدة مع الأعراض السريرية و / أو فرط بيليروبين الدم أو اليرقان أثناء العلاج بـ GOLTOR ، توقف عن العلاج على الفور. إذا لم يتم العثور على مسببات بديلة ، فلا تبدأ العلاج مع GOLTOR.
يجب استخدام GOLTOR بحذر عند المرضى الذين يستهلكون كميات كبيرة من الكحول.
قصور كبدي
نظرًا للتأثيرات غير المعروفة لزيادة التعرض لـ ezetimibe في المرضى الذين يعانون من اختلال كبدي متوسط أو شديد ، لا ينصح باستخدام GOLTOR (انظر القسم 5.2).
السكرى
تشير بعض الأدلة إلى أن العقاقير المخفضة للكوليسترول ، كتأثير طبقي ، تزيد من نسبة الجلوكوز في الدم وفي بعض المرضى ، المعرضين لخطر الإصابة بمرض السكري ، قد يؤدي إلى ارتفاع مستوى السكر في الدم بحيث يكون العلاج المضاد لمرض السكر مناسبًا.
ومع ذلك ، فإن هذا الخطر يفوقه انخفاض مخاطر الأوعية الدموية باستخدام الستاتينات ، وبالتالي لا ينبغي أن يكون سببًا لإيقاف العلاج بالستاتينات.
يجب مراقبة المرضى المعرضين للخطر (الجلوكوز الصائم 5.6 إلى 6.9 مليمول / لتر ، مؤشر كتلة الجسم> 30 كجم / م 2 ، مستويات الدهون الثلاثية المرتفعة ، ارتفاع ضغط الدم) سريريًا وكيميائيًا حيويًا وفقًا للإرشادات الوطنية.
مرضى الأطفال (من 10 إلى 17 سنة)
تم تقييم سلامة وفعالية إيزيتيميب الذي يتم تناوله بالاشتراك مع سيمفاستاتين في المرضى الذين تتراوح أعمارهم من 10 إلى 17 عامًا مع فرط كوليسترول الدم العائلي متغاير الزيجوت في دراسة إكلينيكية مضبوطة على الأولاد المراهقين (مرحلة تانر الثانية أو أعلى) وفي الفتيات. سنة على الأقل.
في هذه الدراسة المحدودة الخاضعة للرقابة ، لم يكن هناك بشكل عام أي تأثير على النمو الجنسي أو النضج عند المراهقين من الفتيان أو الفتيات ، أو أي تأثير على طول الدورة الشهرية عند الفتيات. ومع ذلك ، لم تتم دراسة تأثيرات ezetimibe على مدى فترة العلاج> 33 أسبوعًا على النمو والنضج الجنسي (انظر القسمين 4.2 و 4.8).
لم يتم دراسة سلامة وفعالية إيزيتيميب الذي يتم تناوله بالاشتراك مع جرعات سيمفاستاتين أكبر من 40 ملغ يوميًا في مرضى الأطفال الذين تتراوح أعمارهم بين 10 و 17 عامًا.
لم يتم دراسة Ezetimibe في المرضى الذين تقل أعمارهم عن 10 سنوات أو في الفتيات قبل الحيض (انظر القسمين 4.2 و 4.8).
لم يتم دراسة الفعالية طويلة المدى للعلاج بـ ezetimibe في المرضى الذين تقل أعمارهم عن 17 عامًا لتقليل المراضة والوفيات لدى البالغين.
حزم
لم يتم إثبات سلامة وفعالية دواء ezetimibe المعطى بالفايبرات (انظر أعلاه والأقسام 4.3 و 4.5).
مضادات التخثر
إذا تمت إضافة GOLTOR إلى الوارفارين ، أو مضاد تخثر كومارين آخر ، أو فلوينديون ، فيجب مراقبة نسبة التطبيع الدولية بشكل كافٍ (انظر القسم 4.5).
مرض الرئة الخلالي
تم الإبلاغ عن حالات مرض الرئة الخلالي مع بعض العقاقير المخفضة للكوليسترول ، بما في ذلك سيمفاستاتين ، خاصة مع العلاج طويل الأمد (انظر القسم 4.8). قد تشمل الأعراض ضيق التنفس والسعال غير المنتج وتدهور الصحة العامة (التعب وفقدان الوزن والحمى). إذا اشتبه في أن المريض قد أصيب بمرض رئوي خلالي ، فيجب إيقاف العلاج بـ GOLTOR.
سواغ
المرضى الذين يعانون من مشاكل وراثية نادرة من عدم تحمل الجالاكتوز أو نقص اللاكتاز أو سوء امتصاص الجلوكوز والجالاكتوز يجب ألا يأخذوا هذا الدواء.
04.5 التفاعلات مع المنتجات الطبية الأخرى وأشكال التفاعل الأخرى
التفاعلات الدوائية
التفاعلات مع المنتجات الطبية الخافضة للدهون التي يمكن أن تسبب اعتلال عضلي عند تناولها بمفردها
يزداد خطر الإصابة بالاعتلال العضلي ، بما في ذلك انحلال الربيدات ، أثناء تناول عقار سيمفاستاتين مع الفايبريت. بالإضافة إلى ذلك ، فإن "التفاعل الدوائي لسيمفاستاتين مع جيمفبروزيل يسبب زيادة في مستويات البلازما لسيمفاستاتين (انظر أدناه ، تفاعلات حركية الدواء والأقسام 4.3 و 4.4). ارتبطت حالات نادرة من اعتلال عضلي / انحلال الربيدات بالإعطاء المتزامن للسيمفاستاتين والجرعات المعدلة للدهون من النياسين (1 جم / يوم) (انظر القسم 4.4).
قد يزيد الفايبريت من إفراز الكوليسترول في الصفراء ، مما يؤدي إلى تحص صفراوي ، وفي دراسة ما قبل السريرية على الكلاب ، زاد إزيتيميب من نسبة الكوليسترول في المرارة الصفراوية (انظر القسم 5.3). على الرغم من أن أهمية هذه البيانات قبل السريرية للبشر غير معروفة ، لا ينصح بالإعطاء المتزامن لـ GOLTOR مع الفايبريت (انظر القسم 4.4).
تفاعلات حركية الدواء
تم تلخيص توصيات وصف العوامل المتفاعلة في الجدول التالي (تم تضمين مزيد من التفاصيل في النص ؛ انظر أيضًا الأقسام 4.2 و 4.3 و 4.4).
آثار المنتجات الطبية الأخرى على GOLTOR
جولتور
النياسين: في دراسة أجريت على 15 من البالغين الأصحاء ، أدى الاستخدام المتزامن لـ GOLTOR (10 مجم / 20 مجم يوميًا لمدة 7 أيام) إلى زيادة طفيفة في متوسط قيم AUC للنياسين (22٪) وحمض النيكوتينوريك (19٪). كأقراص NIASPAN ممتدة المفعول (1000 مجم لمدة يومين و 2000 مجم لمدة 5 أيام بعد تناول وجبة إفطار قليلة الدسم). في نفس الدراسة ، أدى الاستخدام المتزامن لـ NIASPAN إلى زيادة طفيفة في متوسط قيم AUC لـ ezetimibe (9٪) ، وإجمالي ezetimibe (26٪) ، و simvastatin (20٪) ، وحمض simvastatin (35٪). القسمين 4.2 و 4.4).
لم يتم إجراء أي دراسات للتفاعل الدوائي مع جرعات أعلى من سيمفاستاتين.
إزتيميب
مضادات الحموضة: أدى التناول المتزامن لمضادات الحموضة إلى خفض معدل امتصاص الإيزيتيميب ولكن لم يكن له أي تأثير على التوافر الحيوي لإيزيتيميب. لا يعتبر هذا الانخفاض في معدل الامتصاص مهمًا من الناحية السريرية.
كوليستيرامين: أدى تناول الكوليسترامين المصاحب إلى خفض متوسط المنطقة الواقعة تحت المنحنى (AUC) لإجمالي ezetimibe (ezetimibe + ezetimibe-glucuronide) بحوالي 55٪. قد يتم تقليل الانخفاض الإضافي في كوليسترول البروتين الدهني منخفض الكثافة (LDL-C) بسبب إضافة GOLTOR إلى الكوليسترامين عن طريق هذا التفاعل (انظر القسم 4.2).
سيكلوسبورين: في دراسة أجريت على ثمانية مرضى بعد زرع الكلى مع تصفية الكرياتينين> 50 مل / دقيقة بجرعات ثابتة من السيكلوسبورين ، أدى إعطاء جرعة واحدة 10 ملغ من إيزيتيميب إلى زيادة قدرها 3.4 أضعاف (نطاق 2.3 - 7.9 مرة) من متوسط AUC لإجمالي ezetimibe مقارنة بمجموعة تحكم صحية من دراسة أخرى تم علاجها باستخدام ezetimibe وحده (ن = 17). في دراسة مختلفة ، أظهر مريض زرع يعاني من قصور كلوي حاد تم علاجه باستخدام السيكلوسبورين والعديد من المنتجات الطبية الأخرى 12 ضعفًا زيادة "إجمالي التعرض لـ" ezetimibe مقارنةً بالضوابط ذات الصلة المعالجة بـ ezetimibe وحده. في دراسة كروس من فترتين ، من بين اثني عشر شخصًا صحيًا ، أدى تناول 20 مجم من ezetimibe يوميًا مع 100 مجم من السيكلوسبورين في اليوم السابع إلى متوسط زيادة بنسبة 15 ٪ في سيكلوسبورين AUC (تتراوح من واحد انخفاض بنسبة 10٪ وزيادة بنسبة 51٪) مقارنة بجرعة واحدة من 100 مجم من السيكلوسبورين وحده. لم يتم إجراء أي دراسات مضبوطة حول تأثير الإعطاء المتزامن لـ ezetimibe على التعرض للسيكلوسبورين في مرضى زرع الكلى.الأخذ المتزامن لـ GOLTOR والسيكلوسبورين هو بطلان (انظر القسم 4.3).
حزم: أدى الاستخدام المتزامن للفينوفيبرات أو الجمفيبروزيل إلى زيادة التركيزات الإجمالية لإيزيتيميب حوالي 1.5 و 1.7 ضعفًا على التوالي. على الرغم من أن هذه الزيادات لا تعتبر مهمة سريريًا ، إلا أن إعطاء GOLTOR المصاحب مع gemfibrozil هو بطلان ولا ينصح باستخدام الفايبرات الأخرى (انظر القسمين 4.3 و 4.4).
سيمفاستاتين
سيمفاستاتين عبارة عن ركيزة من السيتوكروم P450 3A4. تزيد مثبطات السيتوكروم P450 3A4 القوية من خطر الإصابة بالاعتلال العضلي وانحلال الربيدات عن طريق زيادة تركيز نشاط مثبط اختزال HMG-CoA في البلازما أثناء العلاج بسيمفاستاتين. تشمل هذه المثبطات إيتراكونازول ، كيتوكونازول ، بوساكونازول ، فوريكونازول ، إريثروميسين ، كلاريثروميسين ، تيليثروميسين ، مثبطات إنزيم بروتياز HIV (مثل نلفينافير) ، بوسيبريفير ، تيلابريفير ونيفازودون. تسبب تيليثروميسين في زيادة التعرض لحمض سيمفاستاتين بمقدار 11 ضعفًا.
إن المشاركة مع إيتراكونازول ، كيتوكونازول ، بوساكونازول ، فوريكونازول ، مثبطات إنزيم البروتياز لفيروس نقص المناعة البشرية (مثل نلفينافير) ، بوسبريفير ، تيلابريفير ، إريثروميسين ، كلاريثروميسين ، تيليثروميسين ونيفازودون هو بطلان وكذلك مع جيموسبروزيل و 4.3. إذا كان العلاج بمثبطات CYP3A4 القوية (العوامل التي تزيد من AUC حوالي 5 أضعاف أو أكثر) أمرًا لا مفر منه ، يجب التوقف عن العلاج بـ GOLTOR (وينبغي النظر في استخدام الستاتين الآخر) أثناء العلاج ، يجب توخي الحذر عند الجمع بين GOLTOR مع بعض مثبطات CYP3A4 الأخرى الأقل فعالية: فلوكونازول ، فيراباميل ، أو ديلتيازيم (انظر القسمين 4.2 و 4.4).
فلوكونازول: تم الإبلاغ عن حالات نادرة من انحلال الربيدات المرتبطة بالإعطاء المتزامن لسيمفاستاتين وفلوكونازول. (انظر القسم 4.4).
السيكلوسبورين: يزداد خطر الإصابة بالاعتلال العضلي / انحلال الربيدات عن طريق ما يصاحب ذلك من تعاطي سيكلوسبورين مع جولتور ؛ لذلك يُمنع استخدامه مع السيكلوسبورين (انظر القسمين 4.3 و 4.4). على الرغم من أن الآلية غير مفهومة تمامًا ، فقد ثبت أن السيكلوسبورين يزيد من المساحة تحت المنحنى لمثبطات اختزال HMG-CoA. CYP3A4 و / أو OATP1B1.
دانازول: يزداد خطر الإصابة بالاعتلال العضلي وانحلال الربيدات عن طريق ما يصاحب ذلك من تعاطي دانازول مع جولتور ؛ لذلك ، يُمنع استخدامه مع دانازول (انظر القسمين 4.3 و 4.4).
جمفبروزيل: يزيد جيمفبروزيل من المساحة تحت المنحنى للمستقلب الحمضي لسيمفاستاتين بمقدار 1.9 ضعفًا ، ربما بسبب تثبيط الجلوكورونيد و / أو OATP1B1 (انظر القسمين 4.3 و 4.4). هو بطلان الإدارة المصاحبة مع جيمفبروزيل.
حمض الفوسيديك
قد يزداد خطر الإصابة بالاعتلال العضلي بما في ذلك انحلال الربيدات عن طريق التناول المتزامن لحمض الفوسيديك الجهازي مع الستاتينات. قد يؤدي التناول المشترك لهذه المجموعة إلى زيادة تركيزات البلازما لكلا العاملين. لا تزال آلية هذا التفاعل (سواء كانت حركية دوائية أو حركية دوائية أو كليهما) غير معروفة. كانت هناك تقارير عن انحلال الربيدات (بما في ذلك بعض الوفيات) في المرضى الذين يتلقون هذا المزيج. إذا كان العلاج بحمض الفوسيديك مطلوبًا ، يجب التوقف عن العلاج بحمض الفوسيديك طوال مدة العلاج بحمض الفوسيديك (انظر القسم 4.4).
أميودارون: يزداد خطر الإصابة بالاعتلال العضلي وانحلال الربيدات عن طريق التناول المتزامن للأميودارون مع سيمفاستاتين (انظر القسم 4.4). في دراسة سريرية ، تم الإبلاغ عن اعتلال عضلي في 6 ٪ من المرضى الذين عولجوا بسيمفاستاتين 80 ملغ وأميودارون. لذلك ، يجب ألا تتجاوز جرعة GOLTOR 10 مجم / 20 مجم يوميًا في المرضى الذين يتلقون علاجًا مصاحبًا للأميودارون.
حاصرات قنوات الكالسيوم
• فيراباميل: يزداد خطر الإصابة بالاعتلال العضلي وانحلال الربيدات عن طريق الإعطاء المتزامن للفيراباميل مع سيمفاستاتين 40 مجم أو 80 مجم (انظر القسم 4.4).
في دراسة الحرائك الدوائية ، أدى تناول سيمفاستاتين المتزامن مع فيراباميل إلى زيادة قدرها 2.3 ضعف في التعرض لحمض سيمفاستاتين يُفترض أنه يرجع جزئيًا إلى تثبيط CYP3A4. لذلك يجب ألا تتجاوز جرعة GOLTOR 10 مجم / 20 مجم يوميًا في المرضى الذين يتلقون العلاج المصاحب مع فيراباميل.
• الديلتيازيم: يزداد خطر الإصابة بالاعتلال العضلي وانحلال الربيدات عن طريق الإعطاء المتزامن للديلتيازيم مع سيمفاستاتين 80 مجم (انظر القسم 4.4). في دراسة الحرائك الدوائية ، تسبب الإعطاء المتزامن للديلتيازيم والسيمفاستاتين في زيادة 2.7 ضعف في التعرض لحمض سيمفاستاتين ، ربما بسبب تثبيط CYP3A4. لذلك يجب ألا تتجاوز جرعة GOLTOR 10 مجم / 20 مجم يوميًا في المرضى الذين يتلقون العلاج المصاحب مع الديلتيازيم.
• أملوديبين
المرضى الذين يتناولون العلاج المتزامن مع أملوديبين وسيمفاستاتين لديهم مخاطر متزايدة للإصابة بالاعتلال العضلي. في دراسة الحرائك الدوائية ، تسبب التناول المتزامن للأملوديبين في زيادة التعرض لحمض سيمفاستاتين بمقدار 1.6 مرة ، لذلك يجب ألا تتجاوز جرعة GOLTOR 10 مجم / 20 مجم يوميًا في المرضى الذين يتناولون أملوديبين المصاحب.
مثبطات CYP3A4 المعتدلة
المرضى الذين يتناولون منتجات طبية أخرى معروفة بتأثيرها التثبيطي المعتدل على CYP3A4 عند استخدامها بشكل متزامن مع GOLTOR ، خاصة مع الجرعات العالية من GOLTOR ، قد يكون لديهم خطر متزايد للإصابة بالاعتلال العضلي (انظر القسم 4.4).
مثبطات بروتين النقل OATP1B1
حمض سيمفاستاتين هو ركيزة من بروتين النقل OATP1B1. قد يؤدي التناول المتزامن للمنتجات الطبية التي تعتبر مثبطات لبروتين النقل OATP1B1 إلى زيادة تركيزات حمض سيمفاستاتين في البلازما وزيادة خطر الإصابة بالاعتلال العضلي (انظر القسمين 4.3 و 4.4).
عصير جريب فروت: يمنع عصير الجريب فروت السيتوكروم P450 3A4. أدى تناول سيمفاستاتين بكميات كبيرة (أكثر من لتر واحد في اليوم) من عصير الجريب فروت إلى زيادة 7 أضعاف في التعرض لحمض سيمفاستاتين. كما أدى تناول 240 مل من عصير الجريب فروت في الصباح وسيمفاستاتين في المساء إلى زيادة 1.9 مرة ، لذلك يجب تجنب تناول عصير الجريب فروت أثناء العلاج باستخدام GOLTOR.
كولشيسين: كانت هناك تقارير عن اعتلال عضلي وانحلال الربيدات مع ما يصاحب ذلك من تعاطي كولشيسين وسيمفاستاتين في مرضى القصور الكلوي. يُنصح بإجراء مراقبة سريرية دقيقة لمثل هؤلاء المرضى الذين يتناولون هذا المزيج.
ريفامبيسين: بما أن الريفامبيسين محفز قوي لـ CYP3A4 ، فإن المرضى الذين يخضعون لعلاج طويل الأمد بالريفامبيسين (مثل علاج السل) قد يعانون من فقدان فاعلية سيمفاستاتين. في دراسة الحرائك الدوائية على متطوعين أصحاء ، انخفضت المنطقة الواقعة تحت منحنى تركيز البلازما (AUC) لحمض سيمفاستاتين بنسبة 93 ٪ مع ما يصاحب ذلك من تعاطي ريفامبيسين.
النياسينلوحظت حالات اعتلال عضلي / انحلال الربيدات عند تناول سيمفاستاتين مع جرعات معدلة للدهون من النياسين (1 جم / يوم) (انظر القسم 4.4).
آثار الجولتور على الحرائك الدوائية للمنتجات الطبية الأخرى
إزتيميب
في الدراسات قبل السريرية ، تبين أن الإيزيتيميب لا يحفز إنزيمات السيتوكروم P450 المشاركة في استقلاب الدواء. لم يلاحظ أي تفاعلات حركية دوائية مهمة سريريًا بين الإيزيتيميب والأدوية الخاضعة لعملية التمثيل الغذائي بواسطة السيتوكروم P450 1A2 ، 2D6.2C8 ، 2C9 و 3A4 ، أو N- أسيتيل ترانسفيراز.
مضادات التخثر: في دراسة أجريت على اثني عشر رجلاً بالغًا يتمتعون بصحة جيدة ، لم يكن للإعطاء المصاحب لـ ezetimibe (10 مجم مرة واحدة يوميًا) أي تأثير كبير على التوافر الحيوي للوارفارين ووقت البروثرومبين. ومع ذلك ، كانت هناك تقارير ما بعد التسويق عن زيادات في نسبة التطبيع الدولية في المرضى الذين أضافوا ezetimibe إلى الوارفارين أو فلوينديون.إذا تمت إضافة GOLTOR إلى الوارفارين أو أحد مضادات التخثر الكومارين الأخرى ، أو إلى الفلوينديون ، فيجب مراقبة INR بشكل كافٍ ( انظر القسم 4.4).
سيمفاستاتين
سيمفاستاتين ليس له تأثير مثبط على السيتوكروم P450 3A4. لذلك ، لا يُتوقع تأثير سيمفاستاتين على تركيزات البلازما للمواد التي يتم استقلابها عبر السيتوكروم P450 3A4.
مضادات التخثر الفموية: في دراستين سريريتين ، واحدة على متطوعين عاديين والأخرى في مرضى فرط كوليسترول الدم ، سيمفاستاتين 20-40 ملغ / يوم يقوى بشكل معتدل تأثير مضادات التخثر الكومارين. زاد زمن البروثرومبين المُبلغ عنه على أنه نسبة التطبيع الدولية (INR) من خط الأساس 1.7 إلى 1.8 ومن خط الأساس 2.6 إلى 3.4 في المتطوعين ومرضى الدراسة ، على التوالي. تم الإبلاغ عن حالات نادرة جدًا من ارتفاع INR. في المرضى الذين عولجوا بمضادات التخثر الكومارين ، يجب تحديد وقت البروثرومبين قبل بدء العلاج بـ GOLTOR وبشكل متكرر خلال المراحل المبكرة من العلاج لضمان عدم حدوث تغيير كبير في زمن البروثرومبين. بمجرد توثيق زمن البروثرومبين المستقر ، يمكن مراقبة أوقات البروثرومبين على فترات موصى بها بشكل روتيني للمرضى الذين يتناولون مضادات التخثر الكومارين. إذا تم تغيير جرعة GOLTOR أو توقف الإعطاء ، يجب تكرار نفس الإجراء. لم يرتبط علاج Simvastatin بالنزيف أو التغيرات في وقت البروثرومبين في المرضى الذين لا يخضعون للعلاج المضاد للتخثر.
04.6 الحمل والرضاعة
حمل
تصلب الشرايين هو عملية مزمنة ، ويجب أن يكون لإيقاف الأدوية الخافضة للدهون بشكل روتيني أثناء الحمل تأثير ضئيل على المخاطر طويلة الأمد المرتبطة بفرط كوليسترول الدم الأولي.
جولتور
هو بطلان جولتور أثناء الحمل. لا توجد بيانات سريرية متاحة عن استخدام جولتور أثناء الحمل. أظهرت الدراسات التي أجريت على الحيوانات في العلاج المركب سمية إنجابية (انظر القسم 5.3).
سيمفاستاتين
لم يتم التأكد من سلامة عقار سيمفاستاتين عند النساء الحوامل. لم يتم إجراء أي دراسات سريرية خاضعة للرقابة مع سيمفاستاتين في النساء الحوامل. كانت هناك تقارير نادرة عن تشوهات خلقية بعد التعرض داخل الرحم لمثبطات اختزال HMG-CoA. ومع ذلك ، في تحليل مستقبلي لما يقرب من 200 حالة حمل تعرضت خلال الأشهر الثلاثة الأولى من الحمل إلى سيمفاستاتين أو مثبط اختزال HMG-CoA آخر وثيق الصلة ، كان حدوث التشوهات الخلقية مماثلة لتلك التي لوحظت في عامة السكان. كان هذا العدد من حالات الحمل كافياً إحصائياً لاستبعاد حدوث زيادة في التشوهات الخلقية بمقدار 2.5 مرة أو أكبر من الحدوث الأساسي.
على الرغم من عدم وجود دليل على أن حدوث تشوهات خلقية في نسل المرضى الذين عولجوا بسيمفاستاتين أو مثبطات اختزال HMG-CoA الأخرى ذات الصلة الوثيقة تختلف عن تلك التي تظهر في عامة السكان ، فإن علاج الأمهات باستخدام سيمفاستاتين قد يقلل من مستويات الجنين. مقدمة للتخليق الحيوي للكوليسترول. لهذا السبب ، لا ينبغي استخدام GOLTOR في النساء الحوامل ، الراغبات في الحمل أو المشتبه في أنهن حامل. يجب تعليق العلاج بـ GOLTOR طوال فترة الحمل أو حتى لا يتم تحديده أن المرأة ليست حامل (انظر القسم 4.3).
إزتيميب
لا توجد بيانات عن استخدام إيزيتيميب أثناء الحمل.
وقت الأكل
لا يستخدم الجولتور أثناء الرضاعة ، وقد أظهرت الدراسات التي أجريت على الفئران أن الإيزيتيميب يفرز في الحليب. من غير المعروف ما إذا كانت المكونات النشطة لـ GOLTOR تُفرز في لبن الأم (انظر القسم 4.3).
04.7 التأثيرات على القدرة على السياقة واستعمال الآلات
لم يتم إجراء أي دراسات حول التأثيرات على القدرة على القيادة واستخدام الآلات ، ومع ذلك ، عند القيادة أو استخدام الآلات ، يجب أن يؤخذ في الاعتبار أنه تم الإبلاغ عن الدوار.
04.8 الآثار غير المرغوب فيها
تم تقييم سلامة GOLTOR (أو الإدارة المشتركة لـ ezetimibe و simvastatin المكافئ لـ GOLTOR) في حوالي 12000 مريض في الدراسات السريرية.
يتم تصنيف ترددات التأثيرات غير المرغوب فيها على النحو التالي: شائعة جدًا (1/10) ، شائعة ≥ 1/100 ،
لوحظت الآثار غير المرغوب فيها التالية في المرضى الذين عولجوا بـ GOLTOR (N = 2،404) ومع حدوث أعلى من العلاج الوهمي (N = 1،340).
لوحظت الآثار غير المرغوبة التالية في المرضى الذين عولجوا بـ GOLTOR (N = 9595) ومع حدوث أعلى من الستاتين الذي تم إعطاؤه مرة واحدة (N = 8883).
مرضى الأطفال (من 10 إلى 17 سنة)
في دراسة أجريت على مرضى المراهقين (10 إلى 17 عامًا) الذين يعانون من فرط كوليسترول الدم العائلي متغاير الزيجوت (ن = 248) ، لوحظت ارتفاعات في ALT و / أو AST (≥ 3 X ULN ، متتالية) في 3 ٪ (4 مرضى) من المرضى في مجموعة إيزيتيميب / سيمفاستاتين مقابل 2٪ (مريضان) من مجموعة العلاج الأحادي سيمفاستاتين ؛ كانت النسب المئوية للزيادات في قيم CPK (≥ 10 X ULN) 2٪ (2 مريض) و 0٪ على التوالي. لم يتم الإبلاغ عن حالات اعتلال عضلي.
لم تكن هذه الدراسة مناسبة لمقارنة التفاعلات العكسية للأدوية النادرة.
مرضى الكلى المزمنة
في دراسة حماية القلب والكلى (SHARP) (انظر القسم 5.1) ، والتي تشمل أكثر من 9000 مريض عولجوا بـ GOLTOR 10/20 ملغ يوميًا (ن = 4650) أو دواء وهمي (ن = 4620) ، كانت ملفات تعريف السلامة قابلة للمقارنة خلال فترة متوسط فترة المتابعة 4.9 سنوات. في هذه الدراسة ، تم تسجيل الأحداث الضائرة والتوقفات الخطيرة فقط بسبب أي حدث ضار. كانت معدلات التوقف بسبب الأحداث الضائرة قابلة للمقارنة (10.4 ٪ في المرضى الذين عولجوا بـ GOLTOR ، و 9.8 ٪ في المرضى المعالجين بالغفل). كانت نسبة حدوث اعتلال عضلي / انحلال الربيدات 0.2٪ في المرضى الذين عولجوا بـ GOLTOR و 0.1٪ في المرضى الذين عولجوا بدواء وهمي. حدثت ارتفاعات متتالية في الترانساميناسات (> 3x ULN) في 0.7٪ من المرضى. عولج GOLTOR مقابل 0.6٪ من المرضى المعالجين بالغفل في هذه الدراسة ، لم تكن هناك زيادات ذات دلالة إحصائية في حدوث الأحداث الضائرة المحددة مسبقًا ، بما في ذلك السرطان (9.4٪ لـ GOLTOR ، 9.5٪ للعلاج الوهمي) ، التهاب الكبد ، استئصال المرارة أو مضاعفات حصوات المرارة أو التهاب البنكرياس.
التحقيقات التشخيصية
في دراسات الجرعات المركبة ، كان معدل حدوث الارتفاعات المهمة سريريًا في ترانس أميناس المصل (ALT و / أو AST 3 X ULN ، قيم متتالية) 1.7 ٪ في المرضى الذين عولجوا بـ GOLTOR. كانت هذه الارتفاعات بشكل عام بدون أعراض. لا ترتبط بالركود الصفراوي ، وعادت إلى خط الأساس بعد التوقف عن العلاج أو أثناء العلاج (انظر القسم 4.4).
لوحظت زيادات ذات صلة سريريًا في CK (≥ 10 X ULN) في 0.2 ٪ من المرضى الذين عولجوا بـ GOLTOR.
تجربة ما بعد التسويق
تم الإبلاغ عن التأثيرات الإضافية التالية غير المرغوب فيها في استخدام ما بعد التسويق مع GOLTOR أو في التجارب السريرية أو أثناء استخدام ما بعد التسويق مع أحد المكونات الفردية.
اضطرابات الدم والجهاز الليمفاوي: قلة الصفيحات. فقر دم
اضطرابات الجهاز العصبي: اعتلال الأعصاب المحيطية. ضعف الذاكرة
اضطرابات الجهاز التنفسي والصدر والمنصف: السعال. ضيق التنفس؛ مرض الرئة الخلالي (انظر القسم 4.4)
اضطرابات الجهاز الهضمي: الإمساك. التهاب البنكرياس. التهاب المعدة
اضطرابات الجلد والأنسجة تحت الجلد: ثعلبة. حمامي عديدة الأشكال. تفاعلات فرط الحساسية ، بما في ذلك طفح جلدي ، شرى ، تأق ، وذمة وعائية
اضطرابات الجهاز العضلي الهيكلي والنسيج الضام: تقلصات العضلات. اعتلال عضلي * (بما في ذلك التهاب العضلات) ؛ انحلال الربيدات مع أو بدون فشل كلوي حاد (انظر القسم 4.4) ؛ اعتلال الأوتار ، وأحيانًا معقد بسبب التمزق
* في دراسة سريرية ، حدث الاعتلال العضلي بشكل شائع في المرضى الذين عولجوا بسيمفاستاتين 80 ملغ / يوم مقارنة بالمرضى الذين عولجوا بـ 20 ملغ / يوم (1.0٪ مقابل 0.02٪ ، على التوالي) (انظر القسمين 4.4 و 4.5).
اضطرابات التمثيل الغذائي والتغذية: قلة الشهية
اضطرابات الأوعية الدموية: الهبات الساخنة. ارتفاع ضغط الدم
الاضطرابات العامة وظروف موقع الإدارة: ألم
الاضطرابات الكبدية الصفراوية: التهاب الكبد / اليرقان. فشل الكبد القاتل وغير المميت. تحص صفراوي. التهاب المرارة
اضطرابات الجهاز التناسلي والثدي: ضعف الانتصاب
الاضطرابات النفسية: الاكتئاب والأرق
تم الإبلاغ عن متلازمة فرط الحساسية الظاهرة بشكل نادر ، بما في ذلك بعض ما يلي: وذمة وعائية ، متلازمة شبيهة بالذئبة ، ألم العضلات الروماتيزمي ، التهاب الجلد والعضلات ، التهاب الأوعية الدموية ، قلة الصفيحات ، فرط الحمضات ، زيادة معدل ترسيب كرات الدم الحمراء ، التهاب المفاصل وألم المفاصل ، الشرى ، الحمى. أزيز وضيق.
التحقيقات: الفوسفاتيز القلوي المرتفع. اختبار وظائف الكبد غير الطبيعي.
تم الإبلاغ عن زيادة في نسبة HbA1c ومستويات الجلوكوز في الدم أثناء الصيام مع الستاتين ، بما في ذلك سيمفاستاتين.
كانت هناك تقارير نادرة بعد التسويق عن ضعف الإدراك (على سبيل المثال ، فقدان الذاكرة ، النسيان ، فقدان الذاكرة ، ضعف الذاكرة ، الارتباك) المرتبطة باستخدام الستاتين ، بما في ذلك سيمفاستاتين.كانت التقارير بشكل عام غير خطيرة ويمكن عكسها بعد التوقف عن العلاج بالستاتين ، مع أوقات متفاوتة لظهور الأعراض (من يوم إلى سنوات) وحل الأعراض (متوسط 3 أسابيع).
تم الإبلاغ عن الأحداث السلبية الإضافية التالية مع بعض العقاقير المخفضة للكوليسترول:
• اضطرابات النوم بما في ذلك الكوابيس
• العجز الجنسي
• داء السكري: يعتمد تواتره على وجود أو عدم وجود عوامل خطر (جلوكوز الدم الصائم 5.6 مليمول / لتر ، مؤشر كتلة الجسم> 30 كجم / م 2 ، ارتفاع مستويات الدهون الثلاثية ، تاريخ من ارتفاع ضغط الدم).
04.9 جرعة زائدة
جولتور
في حالة الجرعة الزائدة ، يجب استخدام التدابير الداعمة والأعراض. كان الإعطاء المتزامن لـ ezetimibe (1،000 mg / kg) و simvastatin (1،000 mg / kg) جيد التحمل في دراسات السمية الفموية الحادة في الفئران والجرذان. لم يلاحظ أي علامات سريرية للسمية في هذه الحيوانات. كان تقدير الجرعة المميتة النصفية عن طريق الفم لكلا النوعين هو ezetimibe 1،000 mg / kg / simvastatin 1،000 mg / kg.
إزتيميب
في الدراسات السريرية ، كان إعطاء ezetimibe ، 50 مجم / يوم إلى 15 شخصًا صحيًا لمدة تصل إلى 14 يومًا ، أو 40 مجم / يوم إلى 18 مريضًا يعانون من فرط كوليسترول الدم الأولي لمدة تصل إلى 56 يومًا ، جيد التحمل بشكل عام. تم الإبلاغ عن حالات قليلة من الجرعة الزائدة ؛ معظمهم لم يترافق مع آثار جانبية. الآثار الجانبية المبلغ عنها لم تكن خطيرة. في الحيوانات ، لم يلاحظ أي سمية بعد تناول جرعات فموية واحدة مقدارها 5000 مجم / كجم من إيزيتيميب في الجرذان والفئران و 3000 مجم / كجم في الكلاب.
سيمفاستاتين
تم الإبلاغ عن حالات قليلة من الجرعة الزائدة ؛ كانت الجرعة القصوى المأخوذة 3.6 جم. تعافى جميع المرضى دون عواقب.
05.0 الخصائص الصيدلانية
05.1 الخصائص الديناميكية الدوائية
مجموعة العلاج الدوائي: مثبطات اختزال HMG-CoA مع عوامل دوائية أخرى تعمل على تعديل ملف الدهون.
كود ATC: C10BA02.
GOLTOR (إيزيتيميب / سيمفاستاتين) هو منتج خافض للدهون يمنع بشكل انتقائي الامتصاص المعوي للكوليسترول والستيرولات النباتية ذات الصلة ويثبط التوليف الداخلي للكوليسترول.
آلية العمل:
جولتور
يُشتق كوليسترول البلازما من الامتصاص المعوي والتخليق الداخلي ، ويحتوي الجولتور على إيزيتيميب وسيمفاستاتين ، وهما مركبان خافضان للدهون مع آليات عمل تكميلية. يقلل GOLTOR المستويات المرتفعة من الكوليسترول الكلي (إجمالي C) ، LDL-C ، البروتين الشحمي B (Apo B) ، الدهون الثلاثية (TG) ، كوليسترول البروتين الدهني غير عالي الكثافة (C-non-HDL) ، ويزيد من نسبة الكوليسترول المرتفع كثافة البروتين الدهني (HDL-C) من خلال التثبيط المزدوج لامتصاص وتخليق الكوليسترول.
إزتيميب
Ezetimibe يمنع امتصاص الأمعاء للكوليسترول. Ezetimibe نشط عن طريق الفم وله آلية عمل تختلف عن تلك الموجودة في الفئات الأخرى من المواد الخافضة للكوليسترول (مثل الستاتين وعزل حمض الصفراء [الراتنجات] ومشتقات حمض الألياف وستانول النبات). الهدف الجزيئي لـ ezetimibe هو ناقل الستيرول ، Niemann-Pick C1-Like 1 (NPC1L1) ، المسؤول عن امتصاص الأمعاء للكوليسترول والفيتوسترولس.
يتم تحديد Ezetimibe على مستوى حدود الفرشاة للأمعاء الدقيقة ويمنع امتصاص الكوليسترول ، مما يؤدي إلى انخفاض في مرور الكوليسترول المعوي إلى الكبد ؛ يقلل الستاتين من تخليق الكوليسترول في الكبد ، وتنتج هاتان الآليتان المتميزتان انخفاضًا تكميليًا في الكوليسترول. في دراسة سريرية لمدة أسبوعين على 18 مريضًا بفرط كوليسترول الدم ، أدى إيزيتيميب إلى تثبيط امتصاص الأمعاء للكوليسترول بنسبة 54٪ مقارنةً بالدواء الوهمي.
تم إجراء سلسلة من الدراسات قبل السريرية لتحديد انتقائية الإيزيتيميب في تثبيط امتصاص الكوليسترول ، حيث أدى إيزيتيميب إلى تثبيط امتصاص الكوليسترول [14 درجة مئوية] مع عدم وجود تأثير على امتصاص الدهون الثلاثية ، الأحماض الدهنية ، الأحماض الصفراوية ، البروجسترون ، الإيثينيل استراديول ، أو الفيتامينات A و D التي تذوب في الدهون.
سيمفاستاتين
بعد الابتلاع عن طريق الفم ، يتحلل سيمفاستاتين ، وهو لاكتون غير نشط ، في الكبد إلى شكل بيتا هيدروكسي أسيد النشط الذي له نشاط مثبط قوي على اختزال HMG-CoA (اختزال 3-هيدروكسي -3 ميثيل جلوتاريل CoA). يحفز هذا الإنزيم تحويل HMG-CoA إلى ميفالونات ، وهي خطوة مبكرة ومحدودة في التخليق الحيوي للكوليسترول.
لقد ثبت أن Simvastatin يقلل من تركيزات LDL-C الطبيعية والمرتفعة. يتكون LDL من البروتين الدهني منخفض الكثافة (VLDL) ويتم تقويضه بشكل أساسي عن طريق مستقبل LDL عالي التقارب. ينخفض أيضًا البروتين الشحمي B بشكل كبير أثناء العلاج باستخدام سيمفاستاتين. كما يزيد Simvastatin بشكل معتدل من HDL-C ويقلل من TG في البلازما.نتيجة لهذه التغييرات ، يتم تقليل النسب بين إجمالي الكوليسترول / HDL-C و LDL-C / C- HDL.
الدراسات السريرية
في التجارب السريرية الخاضعة للرقابة ، قلل GOLTOR بشكل كبير من إجمالي C و LDL-C و Apo B و TG و non-HDL-C ، وزاد HDL-C في مرضى فرط كوليسترول الدم.
فرط كوليسترول الدم الأساسي
في دراسة مدتها 8 أسابيع ، مزدوجة التعمية ، خاضعة للتحكم الوهمي ، 240 مريضًا يعانون من فرط كوليسترول الدم يخضعون بالفعل للعلاج الأحادي بسيمفاستاتين والذين فشلوا في تحقيق هدف LDL-C وفقًا للبرنامج الوطني لتعليم الكوليسترول (NCEP) (من 2 ، 6 إلى 4.1) مليمول / لتر [100 إلى 160 مجم / ديسيلتر اعتمادًا على خصائص خط الأساس) تم اختيارهم عشوائيًا لتلقي ezetimibe 10 مجم أو دواء وهمي بالإضافة إلى علاج سيمفاستاتين الموجود مسبقًا.لم يصل إلى هدف LDL-C الأساسي (حوالي 80 ٪) ، بشكل ملحوظ حقق المزيد من المرضى الذين تم اختيارهم عشوائياً لإيزيتيميب مع سيمفاستاتين هدف LDL-C عند نقطة نهاية الدراسة مقارنة بالمرضى الذين تم اختيارهم عشوائياً للعلاج الوهمي بالتزامن مع سيمفاستاتين ، 76٪ و 21.5٪ على التوالي.
كانت التخفيضات المقابلة في LDL-C للإيزيتيميب أو الدواء الوهمي المتزامن مع سيمفاستاتين مختلفة بشكل كبير (27 ٪ و 3 ٪ على التوالي).
علاوة على ذلك ، فإن ezetimibe ، الذي يتم تناوله بالتزامن مع علاج simvastatin ، أدى إلى انخفاض كبير في إجمالي C ، Apo B ، TGs مقارنةً بالدواء الوهمي المتزامن مع عقار سيمفاستاتين.
في دراسة متعددة المراكز مزدوجة التعمية لمدة 24 أسبوعًا ، عولج 214 مريضًا يعانون من داء السكري من النوع 2 باستخدام ثيازوليدين ديون (روزيجليتازون وبيوجليتازون) لمدة لا تقل عن 3 أشهر وسيمفاستاتين 20 مجم لمدة 6 أسابيع على الأقل بمتوسط LDL-C 2.4 مليمول / لتر (93 مجم / ديسيلتر) ، تم اختيارهم بصورة عشوائية لتلقي إما سيمفاستاتين 40 مجم أو ما يصاحب ذلك من تعاطي مواد فعالة مكافئة لـ GOLTOR 10 مجم / 20 مجم. كان GOLTOR 10 مجم / 20 مجم أكثر فعالية بشكل ملحوظ من مضاعفة جرعة سيمفاستاتين إلى 40 مجم في تقليل LDL-C (-21٪ و 0٪ على التوالي) ، إجمالي C (-14٪ و -1٪ على التوالي) ، ApoB (-14٪ و -2٪ ، على التوالي) ، و C-non-HDL (-20٪ و -2٪ ، على التوالي) على التخفيضات الملحوظة مع سيمفاستاتين 20 ملغ. نتائج HDL-C و TG بين الاثنين لم تكن مجموعات العلاج مختلفة بشكل كبير ولم تتأثر النتائج بنوع العلاج باستخدام thiazolidinediones.
تم إثبات فعالية نقاط القوة المختلفة لـ GOLTOR (10 مجم / 10 مجم إلى 10 مجم / 80 مجم / يوم) في دراسة متعددة المراكز مدتها 12 أسبوعًا ، مزدوجة التعمية ، خاضعة للتحكم الوهمي ، شملت جميع الجرعات. جميع جرعات سيمفاستاتين ذات الصلة.
عند مقارنة المرضى الذين عولجوا بجميع جرعات GOLTOR مع المرضى الذين عولجوا بجميع جرعات سيمفاستاتين ، قلل GOLTOR بشكل كبير إجمالي C و LDL-C و TG (انظر الجدول 1) وأيضًا Apo B (-42٪ و -29٪ ، على التوالي) و non-HDL-C (-49٪ و -34٪ على التوالي) والبروتين التفاعلي C (-33٪ و -9٪ على التوالي). كانت تأثيرات GOLTOR على HDL-C مشابهة للتأثيرات التي لوحظت مع Simvastatin. أظهر تحليل آخر أن GOLTOR زاد HDL-C بشكل ملحوظ مقارنة بالدواء الوهمي.
الجدول 1
الاستجابة لـ GOLTOR في المرضى الذين يعانون من ارتفاع الكولسترول الأولي
(متوسط التغيير٪ من خط الأساس في غياب العلاج (ب))
(أ) بالنسبة للدهون الثلاثية ، متوسط النسبة المئوية للانحراف عن خط الأساس
(ب) القاعدية - ليست في العلاج بالعقاقير الخافضة للدهون
(ج) جرعات مجمعة من GOLTOR (10 / 10-10 / 80) قللت بشكل كبير من إجمالي C و LDL-C و TG ، مقارنة بسيمفاستاتين ، وزادت HDL-C بشكل ملحوظ مقارنة بالدواء الوهمي.
في دراسة مصممة بشكل مشابه ، كانت النتائج لجميع متغيرات الدهون متسقة بشكل عام. في تحليل مشترك لهاتين الدراستين ، كانت الاستجابة الدهنية لـ GOLTOR متشابهة في المرضى الذين لديهم مستويات TG أكبر من أو أقل من 200 مجم / ديسيلتر.
في تجربة سريرية متعددة المراكز ، مزدوجة التعمية ، خاضعة للرقابة (ENHANCE) ، تم اختيار 720 مريضًا يعانون من فرط كوليسترول الدم العائلي متغاير الزيجوت لتلقي إيزيتيميب 10 مجم بالاشتراك مع سيمفاستاتين 80 مجم (ن = 357) أو سيمفاستاتين 80 مجم (ن = 363) لمدة 2 سنوات. كان الهدف الأساسي من الدراسة هو التحقق من تأثير العلاج المركب ezetimibe / simvastatin على سمك الغلالة الباطنة والوسائط (IMT) للشريان السباتي مقارنة بالسيمفاستاتين وحده. لم يتم إثبات تأثير هذه العلامة بعد. لمراضة القلب والأوعية الدموية والوفيات.
لم تكن نقطة النهاية الأولية ، متوسط تغيير IMT لجميع شرائح الشريان السباتي الستة ، مختلفة بشكل كبير (p = 0.29) بين مجموعتي العلاج بناءً على قياسات الموجات فوق الصوتية في الوضع B. مع ezetimibe 10 mg بالاشتراك مع simvastatin 80 mg أو simvastatin 80 mg وحده ، زاد سمك البطانة الداخلية والسترات الوسطى بمقدار 0.0111 مم و 0.0058 مم ، على التوالي ، على مدار فترة الدراسة التي استمرت عامين (عند خط الأساس ، كان متوسط قياس IMT السباتي 0.68 ملم و 0.69 ملم على التوالي).
ايزيتيميب 10 مجم بالاشتراك مع سيمفاستاتين 80 مجم قلل من LDL-C ، و Total-C ، و Apo B ، و TG أكثر من سيمفاستاتين 80 مجم ، وكانت الزيادة المئوية في C-HDL لمجموعتي العلاج مماثلة. كانت التفاعلات العكسية التي تم الإبلاغ عنها مع ezetimibe 10 mg بالاشتراك مع simvastatin 80 mg متوافقة مع ملف تعريف الأمان المعروف.
يحتوي جولتور على سيمفاستاتين. في تجربتين سريريتين كبيرتين تم التحكم فيهما باستخدام الدواء الوهمي ، دراسة بقاء سيمفاستاتين الاسكندنافية (20-40 مجم ن = 4444 مريض) هـ دراسة حماية القلب (40 ملغ ؛ ن = 20،536 مريضًا) ، تم تقييم تأثير علاج سيمفاستاتين في المرضى المعرضين لخطر الإصابة بأحداث الشريان التاجي بسبب استمرار أمراض القلب التاجية والسكري وأمراض الأوعية الدموية الطرفية وتاريخ السكتة الدماغية أو أمراض الأوعية الدموية الدماغية الأخرى. ثبت أنه يقلل: خطر الوفيات الإجمالية من خلال الحد من الوفيات الناجمة عن أمراض الشرايين التاجية ؛ وخطر الإصابة باحتشاء عضلة القلب غير المميت والسكتة الدماغية ؛ والحاجة إلى الجراحة بإجراءات إعادة تكوين الأوعية التاجية وغير التاجية.
قيمت دراسة فعالية التخفيضات الإضافية في الكوليسترول والهوموسيستين (SEARCH) تأثير العلاج بسيمفاستاتين 80 مجم مقابل 20 مجم (متوسط المتابعة 6.7 سنوات) على أحداث الأوعية الدموية الرئيسية (MVEs ؛ يُعرف بأنه نقص تروية القلب القاتل. المرض ، احتشاء عضلة القلب غير المميت ، إجراء إعادة تكوين الأوعية التاجية ، السكتة الدماغية غير المميتة أو المميتة ، أو إجراء إعادة التوعي المحيطي) في 12064 مريضًا لديهم تاريخ من احتشاء عضلة القلب. لم يكن هناك فرق كبير في حدوث MVEs بين مجموعتين ؛ سيمفاستاتين 20 mg (n = 1،553؛ 25.7٪) مقابل simvastatin 80 mg (n = 1،477؛ 24.5٪)؛ RR 0.94، 95٪ CI: 0.88 to 1، 01. الفرق المطلق في مستوى LDL-C بين المجموعتين على كان مسار الدراسة 0.35 ± 0.01 مليمول / لتر. كانت ملامح الأمان متشابهة بين مجموعتي العلاج باستثناء "حدوث اعتلال عضلي الذي كان حوالي 1.0 ٪ للمرضى المعالجين بـ سيمفاستاتين 80 مجم مقارنة بـ 0.02٪ للمرضى المعالجين بـ 20 مجم. ما يقرب من نصف حالات الاعتلال العضلي هذه حدثت خلال السنة الأولى من العلاج. كانت نسبة حدوث الاعتلال العضلي خلال كل سنة لاحقة من العلاج حوالي 0.1 ٪.
لقد ثبت أن GOLTOR يقلل من الأحداث القلبية الوعائية الرئيسية في المرضى الذين يعانون من أمراض الكلى المزمنة ؛ ومع ذلك ، فإن الزيادة في فائدة GOLTOR على المراضة القلبية الوعائية والوفيات مقارنة بما تم إثباته في simvastatin لم يتم إثباتها بشكل قاطع.
الدراسات السريرية في مرضى الأطفال (من 10 إلى 17 سنة)
في دراسة متعددة المراكز ، مزدوجة التعمية ، خاضعة للرقابة ، 142 فتى (تانر المرحلة الثانية وما فوق) و 106 فتيات بعد الحيض ، تتراوح أعمارهم من 10 إلى 17 عامًا (متوسط العمر 14.2 عامًا) مع فرط كوليسترول الدم العائلي متغاير الزيجوت (إذا كان متغاير الزيجوت) مع LDL-C الأساسي تم اختيار القيم بين 4.1 و 10.4 مليمول / لتر بشكل عشوائي إلى ezetimibe 10 mg بالاشتراك مع simvastatin (10 ، 20 أو 40 mg) أو simvastatin (10 ، 20 أو 40 mg) بمفرده لمدة 6 أسابيع ، ezetimibe و simvastatin 40 mg co - يُدار أو سيمفاستاتين 40 مجم بمفرده لمدة 27 أسبوعًا ، ثم يتم تناول إيزيتيميب وسيمفاستاتين (10 مجم ، 20 مجم ، 40 مجم) لمدة 20 أسبوعًا.
في الأسبوع 6 ، أدى تناول ezetimibe مع سيمفاستاتين (جميع الجرعات) إلى انخفاض كبير في إجمالي C (38٪ مقابل 26٪) ، LDL-C (49٪ مقابل 34٪) ، Apo B (39٪ مقابل 27٪) وغير- HDL-C (47٪ مقابل 33٪) مقابل سيمفاستاتين وحده (جميع الجرعات) كانت النتائج متشابهة بين مجموعتي العلاج لـ TG و HDL-C (-17٪ مقابل -12٪ و + 7٪ مقابل + 6٪ على التوالي) في الأسبوع 33 ، كانت النتائج متوافقة مع نتائج الأسبوع 6 وحقق عدد أكبر بكثير من المرضى الذين تناولوا ezetimibe و simvastatin 40 mg (62٪) "هدفًا علاجيًا مثاليًا وفقًا لـ NCEP AAP (
لم يتم دراسة سلامة وفعالية إيزيتيميب الذي يتم تناوله بالاشتراك مع جرعات سيمفاستاتين أكبر من 40 ملغ يوميًا في مرضى الأطفال الذين تتراوح أعمارهم بين 10 إلى 17 عامًا.لم يتم دراسة الفعالية في المرضى الذين تقل أعمارهم عن 17 عامًا. في الحد من المراضة والوفيات في مرحلة البلوغ.
فرط كوليسترول الدم العائلي متماثل الزيجوت (متماثل اللواقح)
تم إجراء دراسة عشوائية مزدوجة التعمية لمدة 12 أسبوعًا على المرضى الذين يعانون من تشخيص سريري و / أو تشخيص وراثي للـ IF متماثل اللواقح. تم تحليل البيانات من مجموعة فرعية من المرضى (ن = 14) تعامل مع سيمفاستاتين 40 ملغ في الأساس. أدت زيادة جرعة سيمفاستاتين من 40 إلى 80 مجم (ن = 5) إلى انخفاض بنسبة 13٪ في LDL-C من خط الأساس مقارنة بـ 40 مجم سيمفاستاتين. أدى / 80 مجم مجتمعين ، n = 9) إلى انخفاض بنسبة 23٪ في LDL-C من خط الأساس مقارنةً بسيمفاستاتين 40 مجم. في المرضى الذين يتم تناولهم بشكل مشترك مع ezetimibe و simvastatin يعادل GOLTOR (10 مجم / 80 مجم ، ن = 5 ) ، تم إنتاج تخفيض LDL-C بنسبة 29 ٪ من خط الأساس مقارنة مع simvastatin 40 مجم.
الوقاية من أحداث الأوعية الدموية الرئيسية في مرض الكلى المزمن (CKD)
كانت دراسة حماية القلب والكلى (SHARP) عبارة عن دراسة متعددة الجنسيات وعشوائية ومضبوطة بالغفل ومزدوجة التعمية شملت 9438 مريضًا يعانون من أمراض الكلى المزمنة ، كان ثلثهم يخضعون لغسيل الكلى في الأساس. تم تعيين إجمالي 4650 مريضًا في GOLTOR 10/20 و 4620 مريضًا للعلاج الوهمي ، وتبعهم متوسط 4.9 سنوات. كان متوسط عمر المرضى 62 سنة و 63٪ من الذكور و 72٪ قوقازيين و 23٪ مصابين بالسكري ، وبالنسبة لأولئك الذين لا يخضعون لغسيل الكلى ، كان متوسط معدل الترشيح الكبيبي (eGFR) 26.5 مل / دقيقة. / 1.73 م 2. لا يوجد معيار لتضمين الدراسة على أساس الدهون. كان متوسط خط الأساس LDL-C 108 مجم / ديسيلتر. بعد عام واحد ، بما في ذلك المرضى الذين توقفوا عن تناول عقار الدراسة ، انخفض LDL-C بنسبة 26 ٪ مقارنةً بالدواء الوهمي بواسطة simvastatin 20 مجم وحده وبنسبة 38 ٪ من GOLTOR 10/20 ملغ.
كانت المقارنة الأولية المحددة في بروتوكول SHARP هي "تحليل النية إلى العلاج" لأحداث الأوعية الدموية الرئيسية (MVE ؛ يُعرف بأنه احتشاء عضلة القلب غير المميت أو الموت القلبي أو السكتة الدماغية أو أي إجراء لإعادة الأوعية الدموية) فقط في هؤلاء المرضى الذين تم اختيارهم عشوائيًا في البداية إلى GOLTOR (ن = 4،193) أو مجموعات الدواء الوهمي (ن = 4191). تضمنت التحليلات الثانوية نفس المركب الذي تم تحليله للمجموعة العشوائية بأكملها (خط أساس الدراسة أو سنة واحدة) إلى GOLTOR (ن = 4650) أو وهمي (ن = 4620) مثل وكذلك مكونات هذا المركب.
أظهر تحليل نقطة النهاية الأولية أن GOLTOR قلل بشكل كبير من مخاطر الأحداث الوعائية الرئيسية (749 مريض حدث في مجموعة الدواء الوهمي مقابل 639 في مجموعة GOLTOR) مع تقليل نسبي للمخاطر بنسبة 16 ٪ (P = 0.001).
ومع ذلك ، فإن تصميم هذه الدراسة لم يسمح بمساهمة منفصلة من المكون الأحادي ezetimibe في الفعالية للحد بشكل كبير من مخاطر الأحداث الوعائية الرئيسية في المرضى الذين يعانون من CKD.
تظهر المكونات الفردية لـ MVEs في جميع المرضى المعشاة في الجدول 2. قلل GOLTOR بشكل كبير من خطر الإصابة بالسكتة وأي إعادة توعية ، مع عدم وجود فروق عددية مهمة لصالح GOLTOR لاحتشاء عضلة القلب غير المميت والموت القلبي.
الجدول 2
أحداث الأوعية الدموية الرئيسية حسب مجموعة العلاج في جميع المرضى الذين تم اختيارهم عشوائياً في شاربا
تحليل بنية العلاج لجميع مرضى شارب الذين تم اختيارهم عشوائيًا باستخدام GOLTOR أو الدواء الوهمي في الأساس أو في عام واحد
ب ماي ؛ يُعرَّف بأنه مركب من احتشاء عضلة القلب غير المميت ، أو موت الشريان التاجي ، أو السكتة الدماغية غير النزفية ، أو أي إعادة توعية
كان الانخفاض المطلق في كوليسترول LDL الذي تم تحقيقه باستخدام GOLTOR أقل بين المرضى الذين يعانون من انخفاض LDL-C الأساسي (
تضيق الأبهر
كان Simvastatin و Ezetimibe لعلاج تضيق الأبهر (SEAS) عبارة عن دراسة متعددة المراكز ، مزدوجة التعمية ، خاضعة للتحكم الوهمي بمتوسط مدة 4.4 سنوات في 1،873 مريضًا يعانون من تضيق الأبهر بدون أعراض (AS) ، تم توثيقه من خلال معدل تدفق الأبهر الذروة المقاس بواسطة دوبلر بين 2.5 و 4.0 م / ث. تم تسجيل المرضى فقط الذين لم يُعتبر علاج الستاتين ضروريًا لتقليل خطر الإصابة بأمراض القلب والأوعية الدموية المرتبطة بتصلب الشرايين. تم اختيار المرضى بصورة عشوائية بنسبة 1: 1 لتلقي العلاج الوهمي أو ezetimibe 10 ملغ وسيمفاستاتين 40 ملغ يوميا في الإدارة المشتركة.
كانت نقطة النهاية الأولية هي المركب من الأحداث القلبية الوعائية الرئيسية (MCE) التي تتكون من موت القلب والأوعية الدموية ، واستبدال الصمام الأبهري الجراحي (AVR) ، وفشل القلب الاحتقاني (CHF) الناتج عن تطور AS ، واحتشاء عضلة القلب غير المميت ، وتطعيم مجازة الشريان التاجي (CABG). )) ، والتدخل التاجي عن طريق الجلد (PCI) ، والاستشفاء من الذبحة الصدرية غير المستقرة ، والسكتة الدماغية غير النزفية كانت نقاط النهاية الثانوية الرئيسية مجموعات فرعية مركبة من فئات الأحداث لنقطة النهاية الأولية.
مقارنة بالدواء الوهمي ، فإن ezetimibe / simvastatin 10/40 mg لم يقلل بشكل كبير من خطر MCE. حدثت النتيجة الأولية في 333 مريضًا (35.3٪) في مجموعة ezetimibe / simvastatin وفي 355 مريضًا (38.2٪) في مجموعة الدواء الوهمي (نسبة الخطر في مجموعة ezetimibe / simvastatin ، 0.96 ؛ فاصل الثقة 95٪ ، 0.83 إلى 1.12 ؛ p = 0.59) تم إجراء استبدال الصمام الأبهري في 267 مريضًا (28.3٪) في مجموعة ezetimibe / simvastatin وفي 278 مريضًا (29.9٪) في مجموعة الدواء الوهمي (نسبة الخطورة 1.00 ؛ 95٪ CI ، 0.84 إلى 1.18 ؛ p = 0.97) كان لدى عدد أقل من المرضى أحداث قلبية وعائية إقفارية في مجموعة ezetimibe / simvastatin (العدد = 148) مقارنة بمجموعة الدواء الوهمي (n = 187) (نسبة الخطورة ، 0.78 ؛ 95٪ CI ، 0.63 إلى 0.97 ؛ p = 0.02) ، ويرجع ذلك أساسًا إلى إلى عدد أقل من المرضى الذين خضعوا لعملية تطعيم مجازة الشريان التاجي.
حدث السرطان بشكل متكرر في مجموعة ezetimibe / simvastatin (105 مقابل 70 ، p = 0.01). إن الأهمية السريرية لهذه الملاحظة غير مؤكدة حيث أنه في دراسة SHARP الأكبر ، لم يكن العدد الإجمالي للمرضى الذين يعانون من أي نوع من أنواع السرطان الحادث (438 في مجموعة ezetimibe / simvastatin مقابل 439 في مجموعة الدواء الوهمي) مختلفًا ، وبالتالي لم تكن نتيجة SEAS مختلفة. دراسة لا يمكن تأكيدها من قبل شارب.
05.2 خصائص حركية الدواء
لم يلاحظ أي تفاعلات كبيرة في الحرائك الدوائية أثناء الإعطاء المتزامن لـ ezetimibe و simvastatin.
استيعاب :
جولتور
GOLTOR مكافئ بيولوجيًا للإدارة المصاحبة لـ ezetimibe و simvastatin.
إزتيميب
بعد تناوله عن طريق الفم ، يتم امتصاص ezetimibe بسرعة وبشكل مكثف مترافقًا مع الفينول جلوكورونيد النشط دوائيا (ezetimibe-glucuronide). لوحظ متوسط ذروة تركيزات البلازما (Cmax) في غضون ساعة إلى ساعتين لـ ezetimibe-glucuronide و4-12 ساعة لـ ezetimibe. لا يمكن تحديد التوافر الحيوي المطلق لـ ezetimibe لأن المركب غير قابل للذوبان تقريبًا في وسط مائي مناسب للحقن.
لم يكن لتناول الطعام المصاحب (الوجبات الغنية بالدهون أو الخالية من الدهون) أي تأثير على التوافر الحيوي عن طريق الفم لـ ezetimibe المعطى على شكل أقراص 10 مجم.
سيمفاستاتين
وجد أن توافر حمض - -Hydroxy الفعال في الدورة الدموية الجهازية بعد جرعة فموية من سيمفاستاتين أقل من 5٪ من الجرعة ، بما يتوافق مع الاستخراج الكبدي الأول الشامل. - حمض الهيدروكسي وأربعة مستقلبات نشطة أخرى.
لم تتغير ملامح البلازما لكل من المثبطات الكلية والنشطة بإعطاء سيمفاستاتين مباشرة قبل الوجبة القياسية مقارنة بالصيام.
توزيع :
إزتيميب
يرتبط Ezetimibe و ezetimibe-glucuronide بنسبة 99.7٪ و 88-92٪ ببروتينات البلازما البشرية ، على التوالي.
سيمفاستاتين
يرتبط كل من سيمفاستاتين وحمض الهيدروكسي ببروتينات البلازما البشرية (95٪).
لم تظهر الحرائك الدوائية لجرعة واحدة ومتعددة من سيمفاستاتين أي تراكم للأدوية بعد جرعات متعددة. في جميع دراسات الحرائك الدوائية المذكورة أعلاه ، حدث الحد الأقصى لتركيز المثبطات من 1.3 إلى 2.4 ساعة بعد الجرعة.
الإستقلاب :
إزتيميب
يتم استقلاب الإيزيتيميب بشكل أساسي في الأمعاء الدقيقة والكبد عن طريق اقتران الغلوكورونيد (تفاعل المرحلة الثانية) مع إفراز المرارة لاحقًا. لوحظ الحد الأدنى من التمثيل الغذائي التأكسدي (تفاعل المرحلة الأولى) في جميع الأنواع التي تم تقييمها. Ezetimibe و ezetimibe glucuronide هما المركبان الرئيسيان المشتقان من الأدوية الموجودة في البلازما ، ويمثلان ما يقرب من 10-20٪ و 80-90٪ من إجمالي الدواء الموجود في البلازما ، على التوالي. يتم التخلص من كل من ezetimibe و ezetimibe-glucuronide ببطء. من البلازما مع الدليل لدورة معوية كبدية كبيرة يبلغ نصف عمر إيزيتيميب وإيزيتيميب جلوكورونيد حوالي 22 ساعة.
سيمفاستاتين
سيمفاستاتين هو لاكتون غير نشط يتحلل بالماء بسرعة في الجسم الحي في المقابل-هيدروكسي أسيد ، مثبط قوي لانزيم HMG-CoA. يحدث التحلل المائي بشكل رئيسي في الكبد. معدل التحلل المائي في البلازما البشرية بطيء للغاية.
في البشر ، يمتص سيمفاستاتين جيدًا ويخضع لعملية استخراج أولية فورية في الكبد ، ويعتمد الاستخراج في الكبد على تدفق الدم الكبدي. الكبد هو موقع عمله الأساسي ، مع إفراز المواد المكافئة في الصفراء لاحقًا. وبالتالي فإن توافر الدواء الفعال في الدورة الدموية الجهازية منخفض.
بعد إعطاء مستقلب هيدروكسي أسيد عن طريق الوريد ، كان متوسط عمر النصف له 1.9 ساعة.
إزالة :
إزتيميب
بعد تناول 14C ezetimibe عن طريق الفم (20 مجم) في البشر ، يمثل إجمالي ezetimibe حوالي 93 ٪ من إجمالي النشاط الإشعاعي للبلازما. تم استرداد ما يقرب من 78٪ و 11٪ من النشاط الإشعاعي المعطى في البراز والبول ، على التوالي ، خلال فترة جمع العينات لمدة 10 أيام.بعد 48 ساعة ، لم تكن هناك مستويات يمكن اكتشافها من النشاط الإشعاعي في البلازما.
سيمفاستاتين
يتم نقل حمض Simvastatin بنشاط إلى خلايا الكبد عبر الناقل OATP1B1.
بعد تناول جرعة فموية من سيمفاستاتين في البشر ، يتم إفراز 13٪ من النشاط الإشعاعي في البول و 60٪ في البراز خلال 96 ساعة.الكمية الموجودة في البراز تمثل المواد المكافئة التي تفرز في الصفراء وكذلك الدواء غير الممتص بعد إعطاء مستقلب هيدروكسي أسيد في الوريد ، يتم إخراج 0.3٪ فقط من الجرعة الوريدية في البول كمثبطات.
السكان الخاصون:
الأطفال المرضى
يتشابه امتصاص واستقلاب الإيزيتيميب لدى الأطفال والمراهقين (10 إلى 18 عامًا) والبالغين. بناءً على إجمالي ezetimibe لا توجد فروق حركية دوائية بين المراهقين والبالغين.
مرضى الشيخوخة
تركيزات البلازما من إجمالي ezetimibe أعلى مرتين تقريبًا في كبار السن (65 عامًا) كما هو الحال في الشباب (18-45 عامًا). يمكن مقارنة انخفاض LDL-C وملف تعريف الأمان بين كبار السن والأفراد الأصغر سنا الذين عولجوا بـ ezetimibe (انظر القسم 4.2 ).
قصور كبدي
بعد إعطاء جرعة واحدة 10 ملغ من ezetimibe ، زاد متوسط المنطقة الواقعة تحت المنحنى (AUC) لإجمالي ezetimibe 1.7 ضعفًا تقريبًا في المرضى الذين يعانون من اختلال كبدي خفيف (درجة Child Pugh 5 أو 6) ، مقارنة بالأشخاص الأصحاء. في دراسة بجرعة متعددة مدتها 14 يومًا (10 ملغ / يوم) في المرضى الذين يعانون من ضعف كبدي معتدل (درجة الطفل من 7 إلى 9) ، زاد متوسط الجامعة الأمريكية بالقاهرة لإجمالي ezetimibe حوالي 4 مرات يوميًا 1 وفي اليوم 14 مقارنة بالأشخاص الأصحاء. لا حاجة لتعديل الجرعة عند مرضى القصور الكبدي الخفيف. نظرًا للتأثيرات غير المعروفة للتعرض المتزايد لـ ezetimibe في المرضى الذين يعانون من اختلال كبدي متوسط أو شديد (درجة Child Pugh> 9) ، لا ينصح باستخدام ezetimibe في هؤلاء المرضى (انظر القسمين 4.2. و 4.4).
فشل كلوي
إزتيميب
بعد جرعة واحدة 10 ملغ من ezetimibe في المرضى الذين يعانون من مرض كلوي حاد (ن = 8 ؛ يعني CrCl 30 مل / دقيقة) ، زاد متوسط AUC لإجمالي ezetimibe تقريبًا 1.5 مرة مقارنة بالأشخاص الأصحاء. (ن = 9) ، (انظر القسم 4.2).
مريض إضافي في هذه الدراسة (بعد زرع الكلى وعلاجه بالعقاقير المتعددة بما في ذلك السيكلوسبورين) تعرض لـ 12 ضعفًا لـ ezetimibe الكلي.
سيمفاستاتين
في دراسة أجريت على مرضى القصور الكلوي الحاد (تصفية الكرياتينين
الجنس
تراكيز البلازما الكلية للـ ezetimibe أعلى قليلاً (حوالي 20٪) في النساء منها عند الرجال. تقليل LDL-C وملف الأمان يمكن مقارنته بين الرجال والنساء الذين عولجوا بـ ezetimibe.
تعدد الأشكال SLCO1B1
أدت ناقلات الأليل c.521T> C للجين SLCO1B1 إلى تقليل نشاط OATP1B1. متوسط التعرض (AUC) للمستقلب النشط الرئيسي ، حمض سيمفاستاتين ، هو 120٪ في ناقلات متغايرة الزيجوت للأليل C (CT) و 221٪ في حاملات متماثلة اللواقح (CC) مقارنة بالمرضى الذين لديهم النمط الجيني الأكثر شيوعًا (TT) ، الأليل C له تردد 18٪ في سكان أوروبا. هناك خطر من زيادة التعرض لحمض سيمفاستاتين في المرضى الذين يعانون من تعدد الأشكال SLCO1B1 ، مما قد يؤدي إلى زيادة خطر انحلال الربيدات (انظر القسم 4.4).
05.3 بيانات السلامة قبل السريرية
جولتور
في دراسات الإدارة المصاحبة مع ezetimibe و simvastatin ، كانت التأثيرات السامة الملاحظة أساسًا تلك المرتبطة عادةً بالستاتينات. كانت بعض التأثيرات السامة أكثر وضوحًا من تلك التي شوهدت مع علاج الستاتين وحده. يُعزى ذلك إلى التفاعلات الدوائية و / أو الديناميكية الدوائية في الإعطاء المتزامن. لم تحدث تفاعلات من هذا النوع في التجارب السريرية. حدثت نوبات الاعتلال العضلي في الفئران فقط بعد التعرض لجرعات أعلى بعدة مرات من الجرعة العلاجية لدى البشر (حوالي 20 مرة من مستوى AUC لسيمفاستاتين و 1800 ضعف مستوى AUC للمستقلب النشط). لم يكن هناك دليل على أن الإعطاء المتزامن لـ ezetimibe كان له أي تأثير على القدرة السمية العضلية لسيمفاستاتين.
في الكلاب التي يتم تناولها بالاشتراك مع إيزيتيميب والستاتينات ، عند التعرض المنخفض (تضخم القناة الصفراوية ، وتراكم الصباغ ، وتسلل الخلايا أحادية النواة وخلايا الكبد الصغيرة). لم تتطور هذه التغييرات مع التعرض لجرعات طويلة تصل إلى 14 شهرًا. لوحظ انتعاش شامل لنتائج اختبار الكبد بعد التوقف عن التعرض. تتوافق هذه البيانات مع تلك الموصوفة بمثبطات HMG-CoA أو تُعزى إلى مستويات الكوليسترول المنخفضة جدًا التي تحققت في الكلاب قيد الدراسة.
لم يكن التناول المتزامن لـ ezetimibe و simvastatin ماسخًا في الفئران. لوحظ عدد محدود من التشوهات الهيكلية (اندماج الفقرات الذيلية ، انخفاض عدد الفقرات الذيلية) في إناث الأرانب الحوامل.
في سلسلة من المقالات في الجسم الحي و في المختبر لم يُظهر Ezetimibe ، الذي يتم تناوله بمفرده أو بالاشتراك مع simvastatin ، إمكانات السمية الجينية.
إزتيميب
لم تحدد دراسات السمية المزمنة على الحيوانات باستخدام ezetimibe الأعضاء المستهدفة للتأثيرات السامة.في الكلاب التي عولجت لمدة 4 أسابيع بـ ezetimibe (≥ 0.03 مجم / كجم / يوم) زاد تركيز الكوليسترول في الصفراء بعامل 2.5 إلى 3.5. ومع ذلك ، لم يلاحظ أي زيادة في حدوث تحص صفراوي أو تأثيرات كبدية صفراوية أخرى في دراسة الكلاب لمدة عام واحد والتي عولجت بجرعات تصل إلى 300 مجم / كجم / يوم. القيمة السريرية لهذه البيانات بالنسبة للبشر غير معروفة ، ولا يمكن استبعاد خطر تكوين الصخر المرتبط بالاستخدام العلاجي لـ ezetimibe.
كانت اختبارات السرطنة طويلة الأمد على ezetimibe سلبية.
لم يكن لـ Ezetimibe أي تأثير على الخصوبة في أي من الجنسين في الجرذان ، ولم يتم الكشف عن مسخية في الجرذان أو الأرانب ، كما لم يتغير النمو قبل أو بعد الولادة.يعبر Ezetimibe حاجز المشيمة في إناث الجرذان.والأرانب الحوامل التي تلقت جرعات متعددة من 1000 مجم / كجم / يوم.
سيمفاستاتين
بناءً على الدراسات الحيوانية التقليدية للديناميكا الدوائية ، والسمية المتكررة للجرعات ، والسمية الجينية ، والتسرطن ، لا توجد مخاطر على المريض بخلاف تلك المتوقعة على أساس الآلية الدوائية. في الجرعات القصوى التي يمكن تحملها في كل من الجرذان والأرانب ، لم ينتج عن سيمفاستاتين تشوهات جنينية ، ولم يكن له أي تأثير على الخصوبة أو الوظيفة الإنجابية أو نمو الأطفال حديثي الولادة.
06.0 المعلومات الصيدلانية
06.1 السواغات
بوتيل هيدروكسي الأيزول
مونوهيدرات حامض الستريك
الصوديوم Croscarmellose
هيبروميلوز
مونوهيدرات اللاكتوز
ستيرات المغنيسيوم
السليلوز الجريزوفولفين
بروبيل غالات
06.2 عدم التوافق
غير ذات صلة.
06.3 فترة الصلاحية
سنتان.
06.4 احتياطات خاصة للتخزين
لا يجوز التخزين فوق 30 درجة مئوية.
نفطةيحفظ في العلبة الأصلية لحماية الدواء من الضوء والرطوبة.
زجاجات: احفظ الزجاجة مغلقة بإحكام لحماية الدواء من الضوء والرطوبة.
06.5 طبيعة العبوة الفورية ومحتويات العبوة
جولتور 10 مجم / 10 مجم ، 10 مجم / 20 مجم ، 10 مجم / 40 مجم
زجاجة بيضاء من البولي إيثيلين عالي الكثافة (HDPE) مع إغلاق من مادة البولي بروبيلين المقاومة للأطفال وجيل السيليكون المجفف ، ومختومة بعلامة تبويب خاصة ، تحتوي على 100 قرص.
جولتور 10 مجم / 10 مجم
نفطة بولي أميد بولي كلوريد الفينيل / الألومنيوم ملحومة بورق الألمنيوم باستخدام راتنج الفينيل. يمكن استخلاص الأقراص بالضغط على الجيب البلاستيكي عبوات من 7 ، 10 ، 14 ، 28 ، 30 ، 50 ، 56 ، 84 ، 98 ، عبوة متعددة تحتوي على 98 (2 صندوق 49) ، 100 أو 300 قرص.
نفطة أحادية الجرعة من بولي كلوريد الفينيل / بولي أميد الألومنيوم ملحومة بورق الألمنيوم باستخدام راتنج الفينيل. يمكن استخراج الأقراص بالضغط على الجيب البلاستيكي عبوات 30 ، 50 ، 100 أو 300 قرص.
جولتور 10 مجم / 20 مجم ، 10 مجم / 40 مجم
نفطة بولي كلورو ثلاثي فلورو الإيثيلين / بولي كلوريد الفينيل غير شفافة مختومة بورق الألمنيوم باستخدام راتنج الفينيل. يمكن استخراج الاقراص بالضغط على الجيب البلاستيكي عبوة بها 90 قرصا.
جولتور 10 مجم / 20 مجم ، 10 مجم / 40 مجم ، 10 مجم / 80 مجم
نفطة بولي كلورو ثلاثي فلورو الإيثيلين / بولي كلوريد الفينيل غير شفافة مختومة بورق الألمنيوم باستخدام راتنج الفينيل. يمكن استخلاص الأقراص بالضغط على الجيب البلاستيكي عبوات من 7 ، 10 ، 14 ، 28 ، 30 ، 50 ، 56 ، 84 ، 98 ، 100 أو 300 قرص.
جرعة واحدة من البولي كلورو ثلاثي فلورو الإيثيلين / نفطة PVC مختومة بورق الألمنيوم باستخدام راتنجات الفينيل. يمكن استخراج الأقراص بالضغط على الجيب البلاستيكي عبوات 30 ، 50 ، 100 أو 300 قرص.
قد لا يتم تسويق جميع أحجام العبوات.
06.6 تعليمات الاستخدام والتداول
لا توجد تعليمات خاصة.
07.0 حامل ترخيص التسويق
إضافة PHARMA Srl
فيالي شكسبير ، 47
00144 روما
تاجر للبيع:
SIGMA-TAU Industrie Farmaceutiche Riunite S.p.A.
عبر بونتينا كم 30400
00040 بوميزيا (RM)
08.0 رقم ترخيص التسويق
100 قرص في زجاجة من 10 ملغ / 10 ملغ AIC n. 036678011
7 أقراص في عبوات نفطة من 10 ملغ / 10 ملغ AIC n. 036678023
10 أقراص في عبوات نفطة من 10 ملغ / 10 ملغ AIC n. 036678035
14 قرص في عبوات نفطة من 10 ملغ / 10 ملغ AIC n. 036678047
28 قرص في عبوات نفطة من 10 ملغ / 10 ملغ AIC n. 036678050
30 قرص في عبوات نفطة من 10 ملغ / 10 ملغ AIC n. 036678100
50 قرص في عبوات نفطة من 10 ملغ / 10 ملغ AIC n. 036678062
56 قرصًا في عبوات نفطة من 10 ملغ / 10 ملغ AIC n. 036678074
98 قرص في عبوات نفطة من 10 ملغ / 10 ملغ AIC n. 036678086
2 x 49 حبة في عبوات نفطة من 10 ملغ / 10 ملغ AIC n. 036678643
100 قرص في بثور من 10 ملغ / 10 ملغ AIC n. 036678098
300 قرص في عبوات نفطة من 10 ملغ / 10 ملغ AIC n. 036678112
30 قرصًا في بثور أحادية الجرعة 10 مجم / 10 مجم AIC n. 036678124
50 قرصًا في بثور أحادية الجرعة 10 مجم / 10 مجم AIC n. 036678136
100 قرص في 10 ملجم / 10 ملجم بثور أحادية الجرعة AIC n. 036678148
300 قرص في بثور أحادية الجرعة 10 مجم / 10 مجم AIC n. 036678163
100 قرص في زجاجة من 10 ملغ / 20 ملغ AIC n. 036678151
7 أقراص في عبوات نفطة من 10 ملغ / 20 ملغ AIC n. 036678175
10 أقراص في عبوات نفطة من 10 ملغ / 20 ملغ AIC n. 036678187
14 قرص في عبوات نفطة من 10 ملغ / 20 ملغ AIC n. 036678199
28 قرص في عبوات نفطة من 10 ملغ / 20 ملغ AIC n. 036678201
30 قرص في عبوات نفطة من 10 ملغ / 20 ملغ AIC n. 036678213
50 قرص في عبوات نفطة من 10 ملغ / 20 ملغ AIC n. 036678225
56 قرصًا في عبوات نفطة من 10 ملغ / 20 ملغ AIC n. 036678237
98 قرص في عبوات نفطة من 10 ملغ / 20 ملغ AIC n. 036678249
100 قرص في بثور من 10 ملغ / 20 ملغ AIC n. 036678252
300 قرص في عبوات نفطة من 10 ملغ / 20 ملغ AIC n. 036678264
30 قرصًا في 10 ملغ / 20 ملغ بثور أحادية الجرعة AIC n. 036678276
50 قرصًا في 10 مجم / 20 مجم بثور أحادية الجرعة AIC n. 036678288
100 قرص في 10 ملغ / 20 ملغ بثور أحادية الجرعة AIC n. 036678290
300 قرص في 10 ملغ / 20 ملغ بثور أحادية الجرعة AIC n. 036678302
100 قرص في زجاجة من 10 ملغ / 40 ملغ AIC n. 036678314
7 أقراص في عبوات نفطة من 10 ملغ / 40 ملغ AIC n. 036678326
10 أقراص في عبوات نفطة من 10 ملغ / 40 ملغ AIC n. 036678338
14 قرص في عبوات نفطة من 10 ملغ / 40 ملغ AIC n. 036678340
28 قرص في عبوات نفطة من 10 ملغ / 40 ملغ AIC n. 036678353
30 قرص في عبوات نفطة من 10 ملغ / 40 ملغ AIC n. 036678365
50 قرص في عبوات نفطة من 10 ملغ / 40 ملغ AIC n. 036678377
56 قرصًا في عبوات نفطة من 10 ملغ / 40 ملغ AIC n. 036678389
98 قرص في عبوات نفطة من 10 ملغ / 40 ملغ AIC n. 036678391
100 قرص في بثور من 10 ملغ / 40 ملغ AIC n. 036678403
300 قرص في عبوات نفطة من 10 ملغ / 40 ملغ AIC n. 036678415
30 قرصًا في بثور أحادية الجرعة 10 مجم / 40 مجم AIC n. 036678427
50 قرصًا في بثور أحادية الجرعة 10 مجم / 40 مجم AIC n. 036678439
100 قرص في 10 ملغ / 40 ملغ بثور أحادية الجرعة AIC n. 036678441
300 قرص في 10 ملغ / 40 ملغ بثور أحادية الجرعة AIC n. 036678454
7 أقراص في عبوات نفطة من 10 ملغ / 80 ملغ AIC n. 036678466
10 أقراص في عبوات نفطة من 10 ملغ / 80 ملغ AIC n. 036678478
14 قرص في عبوات نفطة من 10 ملغ / 80 ملغ AIC n. 036678480
28 قرصا في بثور من 10 ملغ / 80 ملغ AIC n. 036678492
30 قرص في عبوات نفطة من 10 ملغ / 80 ملغ AIC n. 036678504
50 قرصا في بثور من 10 ملغ / 80 ملغ AIC n. 036678516
56 قرصًا في عبوات نفطة من 10 ملغ / 80 ملغ AIC n. 036678528
98 قرص في عبوات نفطة من 10 ملغ / 80 ملغ AIC n. 036678530
100 قرص في عبوات نفطة من 10 ملغ / 80 ملغ AIC n. 036678542
300 قرص في بثور من 10 ملغ / 80 ملغ AIC n. 036678555
30 قرصًا في بثور أحادية الجرعة 10 مجم / 80 مجم AIC n. 036678567
50 قرصًا في بثور أحادية الجرعة 10 مجم / 80 مجم AIC n. 036678579
100 قرص في 10 ملغ / 80 ملغ بثور أحادية الجرعة AIC n. 036678581
300 قرص في 10 ملغ / 80 ملغ بثور أحادية الجرعة AIC n. 036678593
09.0 تاريخ أول تفويض أو تجديد التفويض
تاريخ أول ترخيص: أغسطس 2005
آخر موعد للتجديد: فبراير 2010
10.0 تاريخ مراجعة النص
مارس 2015












.jpg)